
| m |
| M |
| ||
| 1 |
| 2 |
| n |
| v |
| 3.2g |
| 64g/mol |
| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| n |
| v |
| 0.36mol |
| 0.02L |


科目:高中化学 来源: 题型:
| A、13C与15N具有相同的中子数 |
| B、C60、13C和石墨互为同素异形体 |
| C、等物质的量的13C17O、15N2两种气体具有相同的质子数和原子数 |
| D、13C、15N和C60、N70互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①②④ |
| C、只有③ | D、其它组合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将2mol金属Cu与含2molH2SO4的浓硫酸共热 |
| B、将1 mol MnO2固体与含4molHCl的浓盐酸共热 |
| C、常温下,将32.2g金属钠和5.4g金属铝同时投入到足量水中 |
| D、常温下,将10.8g的Al和22.4g的Fe投入到300g 98%的硫酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
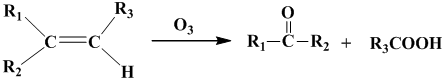
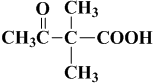
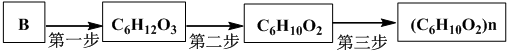
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在硅酸钠溶液中滴加酚酞 |
| B、碳酸钠溶液中滴加酚酞 |
| C、硫酸铁溶液中滴加硫氰化钾溶液 |
| D、碳酸氢钠溶液中滴加稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:

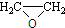 ).写出以邻甲基苯酚(
).写出以邻甲基苯酚(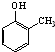 )和乙醇为原料制备
)和乙醇为原料制备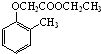 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com