
【题目】甲基、羟基、羧基和苯基,两两结合形成的化合物水溶液的pH小于7(常温下)的有( )
A.5种B.4种C.3种D.2种
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,11.2 L的戊烷所含的分子数为0.5NA
B. 28 g乙烯所含共用电子对数目为4NA
C. 11.2 L二氯甲烷所含分子数为0.5NA
D. 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)双氧水能使酸性高锰酸钾溶液褪色,其反应的化学方程式如下,请将相关的化学计量数填写在方框里:_______□H2O2+□KMnO4+□H2SO4=□MnSO4+□K2SO4+□O2↑+□H2O
(2)某混合溶液中可能含有的离子如下表所示:
可能大量含有的阳离子 | H+、Mg2+、Al3+、NH4+、Fe3+ |
可能大量含有的阴离子 | Cl-、Br-、CO32-、AlO2- |
为探究其成分,进行了以下探究实验。
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠的体积(V)的关系如图所示。
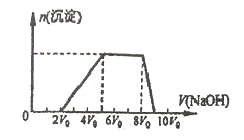
①该溶液中一定含有的阳离子是____________,其对应的物质的量浓度之比为_________,一定不存在的阴离子是______________;
②请写出沉淀减少过程中发生反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某2 L恒容密闭容器中充入2 mol X(g)和1 mol Y(g)发生反应:2X(g)+Y(g)![]() 3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
3Z(g),反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
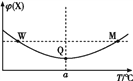
A. M点时,Y的转化率最大
B. 升高温度,平衡常数减小
C. 平衡后充入Z,达到新平衡时Z的体积分数增大
D. W、M两点Y的正反应速率相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们的星球因水而美丽,水也是宝贵的自然资源.
(1)电解水的化学方程式为 .
(2)生活用水在净化过程中常用吸附色素和异味.一般可以通过的方法降低水的硬度.
(3)Fe在高温条件下可与水蒸气反应生成一种单质和一种黑色的氧化物,该氧化物是磁铁矿的主要成分,写出该反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)N2(g)+3H2(g)![]() 2NH3(g);△H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图所示。
2NH3(g);△H=-94.4kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图所示。
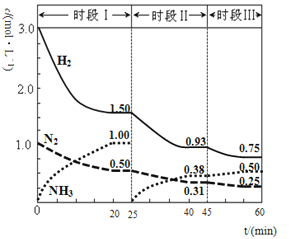
①在1L容器中发生反应,前20min内,v(NH3)=______,放出的热量为________;
②25min时采取的措施是_______;
③时段Ⅲ条件下,反应的平衡常数表达式为____(用具体数据表示,含单位)。
(2)电厂烟气脱氮的主反应①: 4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g),副反应②: 2NH3(g)+8NO(g)
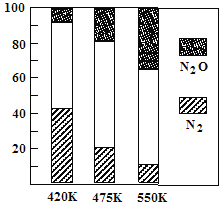
5N2(g)+6H2O(g),副反应②: 2NH3(g)+8NO(g)![]() 5N2O(g)+3H2O(g);△H>0。平衡混合气中N2与N2O含量与温度的关系如图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是________
5N2O(g)+3H2O(g);△H>0。平衡混合气中N2与N2O含量与温度的关系如图。请回答:在400K~600K时,平衡混合气中N2含量随温度的变化规律是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+![]() O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=242kJ·mol1
O2(g)= H2O(g) ΔH3=242kJ·mol1
反应①的ΔH1为________kJ·mol1。
(2)检验硫酸铁溶液中是否存在Fe2+的方法是_______________________________。
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2= 2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的还原剂是_____________,每生成l mol Na2FeO4转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是
A. 质子数相同的原子,其核外电子排布也相同
B. 质量数相同的原子,其化学性质一定相同
C. 金属性越活泼,其原子在反应中越易失去电子
D. 非金属性越活泼,其阴离子越难失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)拆开1 mol H-H键、1 mol N-H键、1 mol N≡N键需要的能量分别是436 kJ、391 kJ、946 kJ,则1 mol N2生成NH3的反应热为__________,1 mol H2生成NH3的反应热为__________。
(2) 写出298 K 101 kPa时,用CO(g)还原1 mol Fe2O3(s),放热24.8 kJ的热化学方程式:________________________________________________________。
(3) 已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1,
N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com