
| |||||||||||||||
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:



 F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F(g)+D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) Fe(OH)3+3H+
Fe(OH)3+3H+ Fe(OH)3+3H+
Fe(OH)3+3H+查看答案和解析>>
科目:高中化学 来源: 题型:
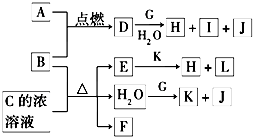 如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
如图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,D的溶液呈棕黄色;组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解



| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释或结论 |
| i | 品红溶液 品红溶液 |
棉球变为白色,微热后又恢复红色 | |
| ii | FeCl3溶液 FeCl3溶液 |
棉球变为浅绿色 | 离子方程式: SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ SO2+2Fe3++2H2O=2Fe3++SO42ˉ+4H+ 结论: SO2有还原性 SO2有还原性 |
| iii | Na2S溶液 | 棉球变为浅黄色 | 解释:浅黄色物质是 S S 结论: SO2有氧化性 SO2有氧化性 |
| iv | 石蕊试液 石蕊试液 |
棉球变为红色 | 化学方程式: SO2+H2O?H2SO3 SO2+H2O?H2SO3 结论:该气体属于酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com