
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
联合国气候变化大会于2009年12月7-18日在哥本哈根召开。中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40 %~45 %。
(1)有效“减碳”的手段之一是节能。下列制氢方法最节能的是 。(填字母序号)
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O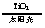 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O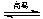 CO+3H2
CO+3H2
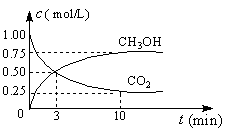 (2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:
(2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,
测得CO2和CH3OH(g)的浓度随时间变化如右图所示。
①写出由CO2和H2制取甲醇的反应的平衡常数
表达式 _
②从3 min到10 min,v(H2)= mol/(L·min)。
③能说明上述反应达到平衡状态的是 (填选项编号)
A.反应中CO2和CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3molH2,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
④下列措施能使n(CH3OH)/(CO2)增大的是 (填选项编号)
A.升高温度 B.恒温恒容充入氦气
C.将水蒸气从体系中分离 D.恒温恒容再充入1 mol CO2和3 mol H2
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
2 CO2(g)+ 6H2(g)→ CH3OCH3(g)+3H2O(l)。有人设想利用二甲醚制作燃料电池,以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是 ( )
A.铝片与稀盐酸反应 B.灼热的炭与二氧化碳反应
C.甲烷在氧气中燃烧 D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
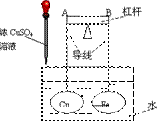 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化) ( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验中,不考虑两球的浮力变化) ( )
A.杠杆为导体或绝缘体时,均为A端高B端低
B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,
A端高B端低
D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在2 L的密闭容器中,X、Y、Z三种气态物质的量随时间的变化曲线如图所示。

(1)由图中所给数据进行分析,该反应的化学方程式为 ____________ ;
(2)反应从开始至2分钟末,用Y的浓度变化表示的平均反应速率为v(Y)= ;
(3)该反应开始时的压强与反应平衡时的压强之比为 ;
(4)X的转化率是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属的说法中,不正确的是 ( )
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.工业上用电解熔融MgCl2的方法制取金属镁
D.铝是活泼金属,但在空气中耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在日常生活、生产中应用广泛。氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。
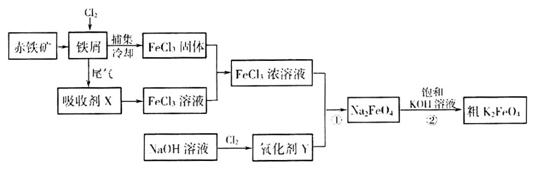 请回答下列问题
请回答下列问题
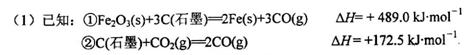
用赤铁矿为原料在高炉炼铁过程中发生的主要反应为
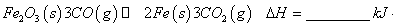 mol
mol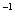 。
。
(2)吸收剂x的溶质为____________(写化学式)。
(3)氧化剂Y为“84消毒液”的有效成分,则在碱性条件下反应①的离子方程式为
__________________________________________________________________
(4)过程②是在某低温下进行的,反应的化学方程式为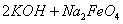 =
=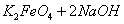 ,说明此温度下
,说明此温度下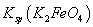 __________
__________ 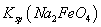 (填“>”或“<”)。
(填“>”或“<”)。
假定此过程中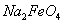 完全转化为
完全转化为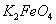 ,若最终制得粗产品
,若最终制得粗产品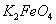 206.25t,产品纯度为96%,则理论上至少需要氧化剂Y的质量是___________t。
206.25t,产品纯度为96%,则理论上至少需要氧化剂Y的质量是___________t。
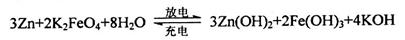 (5)高铁电池是一种新型二次电池,电解液为强碱溶液,其电池反应为:
(5)高铁电池是一种新型二次电池,电解液为强碱溶液,其电池反应为:
放电时电池的负极反应式为______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com