
同温同压下,等质量的O2和CO2相比较,下列叙述错误的是()
A. 密度比为8:11 B. 分子个数之比为11:12
C. 物质的量之比为11:8 D. 原子个数之比为11:12
考点: 阿伏加德罗定律及推论.
分析: 根据阿伏加德罗定律的推论:同温同压下,气体的体积之比等于物质的量之比;同温同压下,气体密度之比等于摩尔质量的之比;同温同压下,分子数之比等于物质的量之比.
解答: 解:A.根据ρ=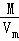 知,同温同压下,其密度之比等于其摩尔质量之比=32g/mol:44g/mol=8:11,故A正确;
知,同温同压下,其密度之比等于其摩尔质量之比=32g/mol:44g/mol=8:11,故A正确;
B.根据N=nNA=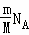 知,相同质量时,其分子数之比等于其摩尔质量的反比,为44:32=11:8,故B错误;
知,相同质量时,其分子数之比等于其摩尔质量的反比,为44:32=11:8,故B错误;
C.由n=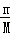 可知,物质的量之比与摩尔质量呈反比,为44:32=11:8,故C正确;
可知,物质的量之比与摩尔质量呈反比,为44:32=11:8,故C正确;
D.根据N=nNA=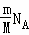 知,等质量的两种气体,其分子数之比与其摩尔质量成反比,所以其分子数之比为44g/mol:32g/mol=11:8,根据每个分子中的原子个数知,其原子个数之比=(11×2):(8×3)=11:12,故D正确.
知,等质量的两种气体,其分子数之比与其摩尔质量成反比,所以其分子数之比为44g/mol:32g/mol=11:8,根据每个分子中的原子个数知,其原子个数之比=(11×2):(8×3)=11:12,故D正确.
故选B.
点评: 本题考查阿伏伽德罗定律及其推论,为2015届高考常见题型,侧重于学生的分析能力和计算能力的考查,难度不大,注意相关计算公式的运用和推导.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
反应 2A=B+3C,在20℃时进行,v(A)=5mol/(L•s),已知每升温10℃,该反应速率增大到原来的2倍,则当其它条件不变而温度升到50℃时,反应速率v(B)是()
A. 20 mol/(L•s) B. 40 mol/(L•s) C. 60 mol/(L•s) D. 15 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为()
A. 1:2:3 B. 3:2:1 C. 6:3:1 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知丙酮(C3H6O)通常是无色液体,易溶于水,密度小于1 g•mL﹣1,沸点约为55℃.要从水与丙酮的混合物中将丙酮分离出来,下列方法中最为合理的是()
A. 蒸馏 B. 分液 C. 过滤 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
在相同的温度和压强下,4个容器中分别装有4种气体.已知各容器中的气体和容器的容积分别是a.CO2,100mL;b.O2,200mL;c.N2,400mL;d.CH4,600mL,则4个容器中气体的质量由大到小的顺序是()
A. a>b>c>d B. b>a>d>c C. c>d>b>a D. d>c>a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
将5mol/L的AlCl3溶液a mL稀释至b mL,稀释后溶液中Cl﹣物质的量浓度为()
A. 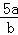 mol/L B.
mol/L B. 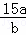 mol/L C.
mol/L C. 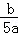 mol/L D.
mol/L D. 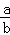 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3纳米)恢复了磁性,“钴酞菁”分子结构和性质与人体的血红素及植物体内的叶绿素非常相似.下列关于“钴酞菁”分子的说法中正确的是()
A. 在水中所形成的分散系属悬浊液
B. 分子直径比Na+小
C. 在水中形成的分散系能产生丁达尔效应
D. “钴酞菁”分子不能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
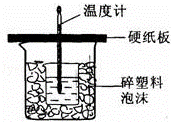
用50mL0.50mol•L﹣1盐酸与50mL0.55mol•L﹣1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器的名称是 .
(2)烧杯间填满碎纸条的作用是 .
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol•L﹣1盐酸与50mL 0.55mol•L﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热相等(填“相等、不相等”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com