
| A. | 简单离子的半径:X<Z<M | |
| B. | Y、R两种元素的气态氢化物稳定性:Y>R | |
| C. | 最高价氧化物对应水化物的酸性:R<N | |
| D. | 由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
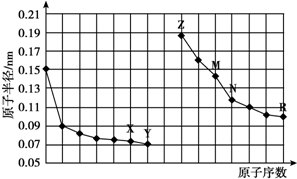
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为F元素,Z为Na元素,M为Al元素,N为Si,R为Cl元素,结合元素周期律与物质的性质等解答.
解答 解:同周期自左而右原子半径减小,同主族自上而下原子半径增大,故前7种元素处于第二周期,后7种元素处于第三周期,由原子序数可知,X为O元素,Y为F元素,Z为Na元素,M为Al元素,N为Si,R为Cl元素.
A.O2-、Na+、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径:O2->Na+>Al3+,故A错误;
B.非金属性F>Cl,非金属性越强氢化物越稳定,故稳定性HF>HCl,故B正确;
C.非金属性Cl>Si,故最高价氧化物对应水化物的酸性:高氯酸>硅酸,故C错误;
D.由X与N两种元素组成的化合物为二氧化硅,能与氢氟酸反应,故D错误,
故选:B.
点评 本题考查位置结构性质的关系及应用,题目难度中等,推断元素是解题的关键,根据原子半径变化规律结合原子序数进行推断,首先审题中要抓住“短周期主族元素”几个字.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g/cm3 | 水中溶解性 |
| 甲 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | -84 | 87 | 0.90 | 可溶 |
| A. | 萃取法 | B. | 升华法 | C. | 蒸馏法 | D. | 分液法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 试管中最终固体为黑色 | B. | 棉花的湿度减小 | ||
| C. | 有肥皂泡产生 | D. | 点燃肥皂泡有轻微爆鸣声 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2S除去废水中的Hg2+:Hg2++S2-═HgS↓ | |
| B. | Na在氧气中燃烧产生淡黄色固体:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2 | |
| C. | 将NO2通入水中,生成硝酸:3NO2+H2O═2H++2NO3-+NO | |
| D. | Al与NaOH水溶液反应产生气体:Al+OH-+2H2O═Al(OH)3↓+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨分解要吸热,可用作制冷剂 | |
| B. | Al2O3难溶于水,可用作耐火坩埚 | |
| C. | 硅胶吸附水能力强,可用作食品干燥剂 | |
| D. | MgO是一种电解质,可用来工业电解冶炼金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上10月阶段测化学卷(解析版) 题型:填空题
化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
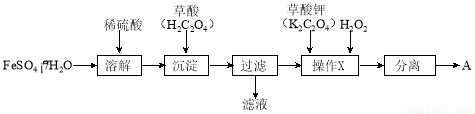
① 上述流程中,检验“过滤”后的固体已洗涤干净的方法是 。
② 上述流程“操作X”中加入H2O2的目的是  。
。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中,加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
通过计算填空,请写出解题过程。
① 4.91g A样品中含结晶水的物质的量为 mol。
② A样品中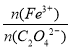 = 。
= 。
③ A的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com