
| A. | 原合金质量为0.92 g | |
| B. | 图中V2为60 | |
| C. | 整个滴定过程中Na+的浓度保持不变 | |
| D. | OP段发生的反应为:NaOH+HCl═NaCl+H2O |
分析 钠铝合金置于水中,合金全部溶解,发生反应:2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,得到20mL pH=14的溶液,则溶液中c(OH-)=1mol/L,NaOH有剩余,剩余NaOH为0.02L×1mol/L=0.01mol;
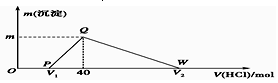
开始加入盐酸没有立即产生沉淀,首先发生反应:NaOH+HCl═NaCl+H2O,该阶段消耗盐酸为$\frac{0.02mol}{1L}$=0.02L=20mL;
然后发生反应:NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,生成氢氧化铝沉淀,40mL时沉淀达最大值,此时溶液中溶质为NaCl,由钠元素守恒可知n(Na)=n(NaCl),该阶段消耗盐酸体积为40mL-20mL=20mL,根据方程式计算n[Al(OH)3],根据铝元素守恒n(Al)=n[Al(OH)3];
最后发生反应:Al(OH)3↓+3HCl═AlCl3+3H2O,
A.根据m=nM计算Na、Al合金的质量;
B.溶解氢氧化铝消耗的盐酸体积与40mL之和为V2的值
C.随盐酸的滴加,溶液体积变大,整个滴定过程Na+的浓度减小;
D.OP段发生反应:NaOH+HCl═NaCl+H2O.
解答 解:钠铝合金置于水中,合金全部溶解,发生反应:2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,得到20mL pH=14的溶液,则溶液中c(OH-)=1mol/L,NaOH有剩余,剩余NaOH为0.02L×1mol/L=0.01mol;
开始加入盐酸没有立即产生沉淀,首先发生反应:NaOH+HCl═NaCl+H2O,该阶段消耗盐酸为$\frac{0.02mol}{1mol/L}$=0.02L=20mL;
然后发生反应:NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,生成氢氧化铝沉淀,40mL时沉淀达最大值,此时溶液中溶质为NaCl,由钠元素守恒可知n(Na)=n(NaCl)=0.04L×1mol/L=0.04mol,该阶段消耗盐酸体积为40mL-20mL=20mL,根据方程式可知n[Al(OH)3]=n(HCl)=0.02L×1mol/L=0.02mol,根据铝元素守恒n(Al)=n[Al(OH)3]=0.02mol,
最后发生反应:Al(OH)3↓+3HCl═AlCl3+3H2O,消耗盐酸的物质的量为0.02mol×3=0.06mol,故该阶段消耗的盐酸体积为$\frac{0.06mol}{1mol/L}$=0.06L=60mL,
A.由上述分析可知,Na、Al合金的质量为0.04mol×23g/mol+0.02mol×27g/mol=1.46g,故A错误;
B.由上述计算可知,溶解氢氧化铝消耗盐酸的体积为60mL,则V2为40mL+60mL=100mL,故B错误;
C.随盐酸的滴加,溶液体积变大,整个滴定过程Na+的浓度减小,而不是不变,故C错误;
D.OP段发生反应:NaOH+HCl═NaCl+H2O,离子方程式为:OH-+H+═H2O,故D正确;
故选D.
点评 本题考查混合物的有关计算,明确发生的化学反应及反应与图象的对应关系是解答本题的关键,注意利用元素守恒的方法来解答,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 若使电解质溶液恢复到电解前的浓度可向溶液中加入9.8×(10-b-10一a)g Cu(OH)2 | |
| B. | b<a<7 | |
| C. | 阳极产生的气体是O2,其体积(标准状况下)为:1.12×(10-b-10-a)L | |
| D. | 阴极电极反应式为:Cu2++2e-=Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,若电解5min时铜电极质量 增加2.16g,试回答:
如图所示,若电解5min时铜电极质量 增加2.16g,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、O2、CO、NH3 | B. | H2、O2、SO2、NH3 | C. | H2、Cl2、HCl、NH3 | D. | NO、O2、NO2、NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是具有丁达尔现象 | |
| B. | 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 | |
| C. | 根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等 | |
| D. | 强电解质溶液的导电能力一定强于弱电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.5×10-4m mol | B. | 5.0×10-4m mol | C. | 7.5×10-4m mol | D. | 1×10-3m mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将二氧化碳通过过氧化钠使其增重ag 反应中转移电子数为 $\frac{a{N}_{A}}{14}$ | |
| B. | 1mol Cl2 通入水中,则n(HClO)+n(Cl-)+n(ClO-)=2NA | |
| C. | 常温常压下,3克含甲醛的冰醋酸中含有的原子总数为0.4NA | |
| D. | 2.24升的甲烷中含有的C-H键数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{(1{0}^{-8}+1{0}^{-10})}{2}$mol/L | B. | (10-8+10-10)mol/L | ||
| C. | (10-14-5×10-5)mol/L | D. | 2×10-10 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com