
分析 (1)根据质量和原子守恒,焦炭与水蒸气高温下反应生成两种可燃性气体,据此书写方程式;
(2)据热化学方程式和盖斯定律计算;
(3)结合平衡三段式列式计算平衡浓度,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积得到;
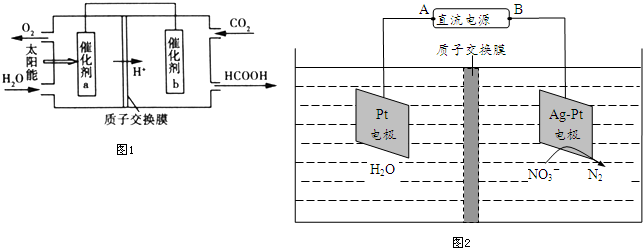
(4)由图可知,左室投入是水,生成氧气与氢离子,催化剂a表面发生氧化反应,为负极,右室催化剂b表面通入二氧化碳,酸性条件下生成HCOOH,电极反应式为CO2+2H++2e-=HCOOH;
(5)该装置中,硝酸根离子得电子发生还原反应,则Ag-Pt电极为阴极,反应式为2NO3-+6H2O+10e-=N2↑+12OH-,Pt电极为阳极,连接阳极的电极为正极,据此分析计算.
解答 解:(1)根据质量和原子守恒,焦炭与水蒸气高温下反应生成两种可燃性气体为CO和H2,则反应的方程式为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,故答案为:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2;
(2)①2CO(g)+O2(g)=2CO2(g)△H1=-566kJ?mol-1
②2NO(g)+2CO(g)?N2(g)+2CO2(g)△H2=-746kJ?mol-1
依据盖斯定律计算①-②得到反应的热化学方程式为:N2(g)+O2(g)=2NO(g),△H=(-566+746)=+180KJ/mol,
故答案为:+180;
(3)在一定温度下,向1L密闭容器中充入0.5mol NO、2mol CO,发生上述反应②,20S反应达平衡,此时CO的物质的量为1.6mol,依据化学平衡三段式列式计算:
2NO(g)+2CO(g)?N2(g)+2CO2(g)
起始量(mol) 0.5 2 0 0
变化量(mol) 0.4 0.4 0.2 0.4
平衡量(mol) 0.1 1.6 0.2 0.4
体积为1L,物质的量数值为浓度数值,计算得到平衡常数K=$\frac{0.2×0.4{\;}^{2}}{0.1{\;}^{2}×1.6{\;}^{2}}$=1.25;
故答案为:1.25;
(4)由图可知,左室投入是水,生成氧气与氢离子,催化剂a表面发生氧化反应,为负极,右室催化剂b表面通入二氧化碳,酸性条件下生成HCOOH,电极反应式为CO2+2H++2e-=HCOOH,故答案为:CO2+2e-+2H+=HCOOH;
(5)根据图知,电解槽右边部分N元素化合价由+5价变为0价,所以硝酸根离子发生还原反应,则Ag-Pt电极为阴极,反应式为2NO3-+6H2O+10e-=N2↑+12OH-,Pt电极为阳极,所以A是正极;又转移了0.4mol电子,根据阴极反应式,则消耗的硝酸根为$\frac{0.4}{10}$×2×62=4.96g,故答案为:A;4.96.
点评 本题考查了热化学方程式的书写方法,化学平衡的计算分析判断,原电池和电解池的原理的分析与计算,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 决定元素种类的是--电子数 | |
| B. | 决定元素化学性质的是--原子的核外电子数 | |
| C. | 决定元素相对原子质量的是--中子数 | |
| D. | 决定元素周期表中原子序数的是--核电荷数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B与C形成的化合物的电子式为
,B与C形成的化合物的电子式为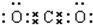 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同的催化剂对化学反应速率影响均相同 | |
| B. | 新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展远景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
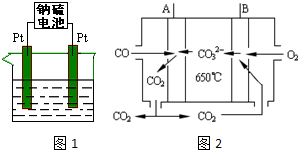
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
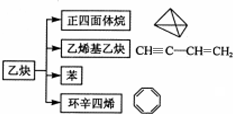
| A. | 图中五种有机物的实验式相同 | |
| B. | 乙炔生成乙烯基乙炔是加成反应 | |
| C. | 等质量的苯与乙烯基乙炔完全燃烧的耗氧量不同 | |
| D. |  与环辛四烯均能使溴水褪色 与环辛四烯均能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
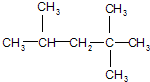 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简 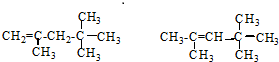 .
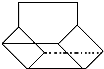
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com