
| A、Na+、Mg2+、NO3-、SO42- |
| B、Ba2+、K+、Cl-、SO42- |
| C、Fe2+、Na+、Cl-、NO3- |
| D、K+、Ca2+、CH3COO-、HCO3- |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1.0 | 2.0 | 3.0 | |
| 810 | 54.0 | - | a |
| 915 | - | 75.0 | - |
| 1000 | - | b | 83.0 |
| A、△S<0 |
| B、915℃2.0MPa,A的转化率为60% |
| C、a>b |
| D、平衡常数:K(1000℃)<K(810℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 实验数据(mL) | 1 | 2 | 3 |
| V(样品) | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 14.95 | 15.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:
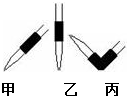 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 23.54 | 20.00 |
| 2 | 0.10 | 23.96 | 20.00 |
| 3 | 0.10 | 24.00 | 20.00 |
| 4 | 0.10 | 24.04 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com