
| A. | OH-+AlO2-+2H+=Al(OH)3 | B. | OH-+AlO2-+5H+=Al3++3H2O | ||
| C. | 2OH-+AlO2-+3H+=Al(OH)3+H2O | D. | OH-+2AlO2-+3H++H2O=2Al(OH)3 |
分析 溶液中c(NaOH)=2c(NaAlO2),则n(NaOH)=2n(NaAlO2),向该溶液中加入HCl后,NaOH优先反应,HCl少量时只发生反应:OH-+H+=H2O;当氢氧根离子完全反应后,AlO2-离子才开始反应,所以AlO2-反应时,发生总反应为:2OH-+AlO2-+3H+=Al(OH)3↓+H2O,据此进行解答.
解答 解:溶液中c(NaOH)=2c(NaAlO2),则n(NaOH)=2n(NaAlO2),向该溶液中加入HCl后,NaOH优先反应;当氢氧根离子完全反应后,AlO2-离子才开始反应,所以AlO2-若参与反应时,OH-离子的物质的量至少为偏铝酸根离子的2倍,发生总反应为:2OH-+AlO2-+3H+=Al(OH)3↓+H2O,
A.OH-离子优先结合氢离子,由于n(NaOH)=2n(NaAlO2),则不可能发生OH-+AlO2-+2H+=Al(OH)3↓,故A错误;
B.n(NaOH)=2n(NaAlO2),氢氧根离子反应完全前氢氧化铝沉淀不会溶解,故B错误;
C.根据分析可知,可能发生反应2OH-+AlO2-+3H+=Al(OH)3↓+H2O,故C正确;
D.n(NaOH)=2n(NaAlO2),氢氧根离子优先反应,则不会发生反应OH-+2AlO2-+3H++H2O=2Al(OH)3↓,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,明确发生反应的先后顺序为解答关键,试题有利于提高学生的分析能力及灵活应用能力.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| B. | 在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声 | |
| C. | 制氧气时排水法收集氧气后出现倒吸现象,应立即松开试管上的橡皮塞 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃同系物随着相对分子质量增大,熔点、沸点逐渐升高 | |
| B. | 烷烃都能使溴水、酸性KMnO4溶液褪色 | |
| C. | 烷烃跟卤素单质在光照条件下能发生取代反应 | |
| D. | 烷烃同系物的密度随着相对分子质量的增大逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
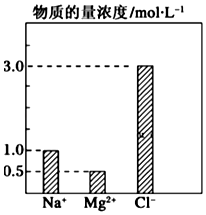 在0.2L由NaCl、MgCl2、BaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、BaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的燃烧产物对大气无污染,因此它是一种优良的燃料 | |
| B. | 乙醇能与钠反应放出氢气,所以它是电解质 | |
| C. | 0.9%的乙醇可用于杀菌、消毒 | |
| D. | 甲醇和乙醇有相似的气味,均可用于配制饮用酒和调味用的料酒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
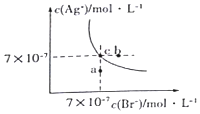 在t°C时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t°C时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t°C时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t°C时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A. | 图中a点对应的是AgBr的不饱和溶液 | |
| B. | 在t°C时,AgBr的Ksp为 4.9×10-13 | |
| C. | 在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点 | |
| D. | 在t°C时,AgCl(s)+Br-(aq)?AgBr(s)+C1-(aq)的平衡常数K≈816 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com