
【题目】NaH2PO2可用于化学镀镍,常通过反应“P4+3NaOH+3H2O==3NaH2PO2+PH3↑”制得,产物PH3中P的化合价为-3。下列说法正确的是
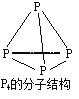
A.P4分子中含有的共价键是极性键
B.31g P4中所含P-P键的物质的量为6 mol
C.反应中还原剂和氧化剂的物质的量之比为1∶3
D.反应生成2.24 L PH3(标准状况),转移电子数目为0.3×6.02×1023
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:
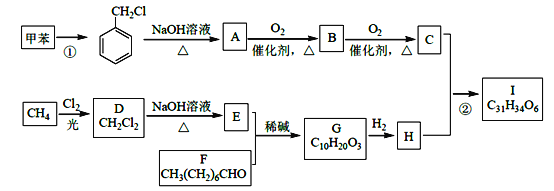
已知:a、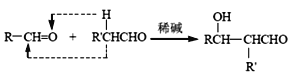
b、
回答下列问题:
(1)反应①所需试剂、条件分别是____________;F 的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)E的结构简式为______________;H 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件,W 的可能结构有____种。①遇FeCl3 溶液显紫色;②能发生银镜反应,其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式____________。
(5)设计用甲苯和乙醛为原料制备![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A![]() B。。。
B。。。![]() 目标产物。____________。
目标产物。____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是)
选项 | 已知 | 类推 |
A | 将Fe加入CuSO4溶液中:Fe+Cu2+=== Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+Cu2+=== Cu+2Na+ |
B | 向Ca(ClO)2溶液中通入少量CO2:CO2+H2O+Ca2++2ClO-=== CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:SO2+H2O+Ca2++2ClO-=== CaSO3↓+2HClO |
C | 惰性电极电解氯化钠溶液:2Cl-+2H2O | 惰性电极电解MgBr2溶液:2Br-+2H2O |
D | 稀盐酸与NaOH溶液反应至中性:H++OH-===H2O | 稀硝酸与Ba(OH)2溶液反应至中性:H++OH-===H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的前三周期及其中的部分元素,请回答相关问题

(1)a、f、g元素最高价氧化物的水化物碱性由强到弱的顺序是____(用化学式表示)。
(2)氢元素可与其它元素形成_____(填选项序号)等化学键。
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为_____,向该化合物的水溶液中加入盐酸发生自身歧化反应的离子方程式为______。
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为______,分液时有机层应从______(填“下口流出“或“上口倒出”)。该有机溶剂的电子式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铁红(Fe2O3)用途广泛,用废铁皮制取铁红的部分流程示意图如下:
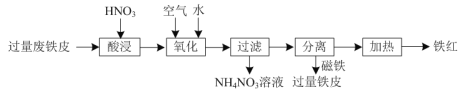
⑴“酸浸”时发生反应的离子方程式是______。
⑵“氧化”时有红褐色沉淀生成,该反应的离子方程式为______。
⑶将铁红与FeS2混合焙烧可以生成磁性氧化铁和SO2,该反应的化学方程式为______。
⑷“淬火”是将红热的铁器浸入水中急速冷却以增加铁器的硬度以及减缓腐蚀,反应历程如图,写出该历程中第Ⅰ步反应的方程式______。
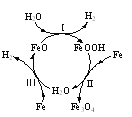
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质结构的命题中,错误的项数有( )
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于P区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2中阴阳离子个数比不同
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:
⑦HF晶体沸点高于HCl,是因为 HCl共价键键能小于HF
A. 4项B. 5项C. 6项D. 7项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杀灭菊酯是一种高效低毒农药,一种合成杀灭菊酯的路线如下:
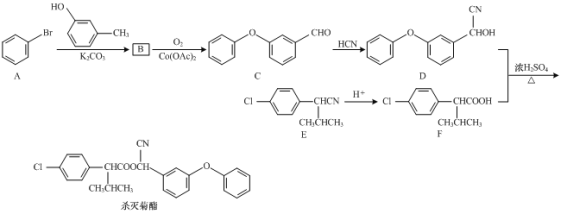
⑴C中含氧官能团的名称为______和______。
⑵B的分子式为C13H12O,则B的结构简式为______。
⑶B→C的反应类型为______。
⑷任写出一种符合下列要求的化合物C的同分异构体的结构简式:______。
Ⅰ既能发生银镜反应,也能发生水解反应,酸性条件下所得水解产物之一核磁共振氢谱中有6个峰;Ⅱ分子中含有2个苯环。
⑸写出以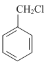 为原料制备
为原料制备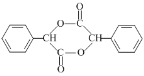 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。__________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 氯水中有平衡:Cl2+H2O![]() HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B. 对CO(g)+NO2(g)![]() CO2(g)+NO(g),平衡体系增大压强可使颜色变深
CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C. 对2NO2(g)![]() N2O4(g) △H<0, 升高温度平衡体系颜色变深
N2O4(g) △H<0, 升高温度平衡体系颜色变深
D. SO2催化氧化成SO3的反应,往往加入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.92 g铜跟适量的浓硝酸反应,铜全部作用后,共收集到1.12 L标准状况下的气体(假设只有NO2、NO),则反应消耗的硝酸的物质的量可能是
A.0.11 molB.0.1 molC.0.09 molD.0.08 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com