
Χ�������������ʣ���������A12O3����ϡ���ᣬ��H2SO4����Ba(OH)2���壬����ˮ����A12(SO4)3������Ҫ��ش��������⡣
��1��������ǿ�ᷴӦ��������ǿ�Ӧ���� ������ţ���
��2�����ڵ���ʵ��� ������ţ���
��3��д����������ȡAl(OH)3�����ӷ���ʽ ��
��4�������ʷ�����Ӧ�����ӷ���ʽΪH++OH��=H2O����д���÷�Ӧ�Ļ�ѧ����ʽ ��
��5��34.2g������ˮ���500mL��Һ����Һ��SO42�������ʵ���Ũ��Ϊ ��
��6��������������Ӧ�Ļ�ѧ����ʽΪA1+4HNO3=A1(NO3)3+NO��+2H2O���÷�Ӧ�л�ԭ���������������ʵ���֮���� ��
��1���٢�����1�֣����1����0.5�֣����һ�������֣�
��2���ڢܢݢ�����2�֣����1����0.5�֣����һ�������֣�
��3��Al3����3NH3��H2O=Al(OH)3����3NH4������2����
��4��2HNO3+Ba(OH)2= Ba(NO3)2+2H2O����2����
��5��0.6mol/L����2�֣���λδд��0.5�֣�
��6��1��1����1�֣�
��������
�����������1��Al��Al2O3������ǿ�ᷴӦ��������ǿ�Ӧ����2���������ᡢ��Ρ��������������ڵ���ʣ����ʡ�����Һ������Һ���ǵ���ʣ���3��ʵ���ҳ���������Һ�백ˮ��ȡAl(OH)3��Al3����3NH3��H2O=Al(OH)3����3NH4������4��H++OH��=H2O����ǿ����ǿ�������ɿ������κ�ˮ���кͷ�Ӧ��2HNO3+Ba(OH)2= Ba(NO3)2+2H2O����5����m/M��֪��n[A12(SO4)3]=0.1mol����A12(SO4)3��3SO42����֪��n(SO42��)=0.3mol����n/V��֪��c(SO42��)=0.6mol/L����6����Ԫ��ȫ����0�����ߵ�+3�ۣ�����������Al�ǻ�ԭ����1/4��Ԫ����+5�۽��͵�+2�ۣ�����ԭ����HNO3������������÷�Ӧ�л�ԭ����������֮��Ϊ1��1��
���㣺������Ԫ�ػ��������ʡ����ӷ���ʽ�����ʵ��������ʵ���Ũ�ȡ���ԭ���������������֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�콭���Ͼ��и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
3��22���� ������ˮ���������и���Ӧ�У�ˮ��Ϊ��ԭ������
A��2H2+O2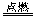 2H2O B��SO3+H2O=H2SO4
2H2O B��SO3+H2O=H2SO4
C��2F2+2H2O=4HF+O2 D��2Na+2H2O=2NaOH+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ÷���и�һ��ѧ���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ���� ( )
A��ͬ����Ԫ���У�VII A��Ԫ�ص�ԭ�Ӱ뾶���
B�����ѷ��ֵ�����Ԫ�صĵ����ڳ��³�ѹ�¶�������
C��VI A��Ԫ�ص�ԭ�ӣ���뾶Խ��Խ���õ�����
D�����е�����Ԫ�صļ����ӵĻ��ϼ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�FeCl3��Һ��Fe(OH)3����������ȷ����
A����FeCl3��Һ��Fe(OH)3�����м��뱥��NaCl��Һ������������
B������ֽ���˷���FeCl3��Һ��Fe(OH)3����Ļ����
C��FeCl3������Һ��NaOHŨ��Һ��ϼ����Ʊ��õ�Fe(OH)3����
D����Fe(OH)3��������ε��������Ȳ���������������ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ɽ��������⻯ѧ�Ծ��������棩 ���ͣ������
��1.66g̼���ƺ��������ƵĹ���������ȫ����ˮ�����ϡ��Һ��Ȼ�������Һ����μ���1mo1/L�����ᣬ�������������������CO2���������״������ϵ��ͼ��ʾ��
��ʾ��Na2CO3�������Ƿֲ����еģ���һ��ΪNa2CO3+HCl=NaHCO3+NaCl���ڶ���ΪNaHCO3+HCl=NaCl+H2O+CO2����
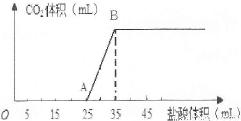
��ش��������⣺
��1��OA����������Na2CO3��NaOH�����ķ�Ӧ����Ӧ����Һ�е������� (�ѧʽ)��
��2��������B��ʱ������CO2�����Ϊ mL(��״��)��
��3������ԭ�������Na2CO3������������(д��������̣��������С�����һλ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ɽ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��FeCl3��CuSO4��Һ�м�����������ۣ������˺�ⶨ��Ӧǰ����Һ���������䣨���ƹ�����ʧ������ԭ����Һ��FeCl3��CuSO4�����ʵ���֮��Ϊ
A��1��1 B��2��1 C��1��7 D��2��7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ɽ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
12��2��1ʱ30�֣����϶�����������̽��������ɹ������϶�������װ�е��ˮ������װ�ã����ṩ����̽��ϵͳ����Ҫ�ĸߴ���������Χ�Ʒ�Ӧ����ʽ2H2O 2H2��+O2���������й��ж���ȷ����
2H2��+O2���������й��ж���ȷ����
A������������Ԫ��
B����ԭ������O2
C��H2O����������Ҳ�л�ԭ��
D��2molH2O��Ӧ��ת����8mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ݸ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ���A���������棩 ���ͣ�ѡ����
������ʵ����ʵ�ó�������������
A�������Ǽ���Ũ������ڣ�˵��Ũ���������ˮ��
B��Ũ�������������������˵��Ũ���������ˮ��
C��ͭ��Ũ���Ṳ���д̼�����ζ����ų���˵��Ũ�������ǿ������
D��������Ũ��������������棬˵���������Ũ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ˷���и�һ��ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ҩƷ���ô����������Լ�ƿ��ŵ���
A������ B������� C��NaOH��Һ D. Na2SiO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com