
| A. | 铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线绞接在一起 | |
| B. | 汽车尾气中含有能污染空气的氮的氧化物,原因是汽油燃烧不充分 | |
| C. | 用新制备的Cu(OH)2悬浊液与病人尿液共热,可检验病人尿液中是否含有葡萄糖 | |
| D. | 某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2 |
分析 A.活泼性不同的金属遇到合适的电解质溶液易构成原电池而腐蚀金属;
B.气缸中的氮气被氧化生成氮的氧化物;
C.新制氢氧化铜悬浊液能和葡萄糖反应生成砖红色沉淀;
D.亚硫酸容易被空气中氧气氧化生成硫酸.
解答 解:A.铝和铜具有良好的导电性,但铜和铝遇到合适的电解质溶液能构成原电池而发生金属铝,所以所以电工操作时,不能把铜线和铝线绞接在一起,故A错误;
B.气缸中的氮气在高温下被氧气氧化生成氮的氧化物,汽油不充分燃烧生成一氧化碳,故B错误;
C.糖尿病人的尿液中含有葡萄糖,葡萄糖含有醛基,新制的氢氧化铜悬浊液能和葡萄糖反应生成砖红色沉淀,所以可以用新制备的Cu(OH)2悬浊液与病人尿液共热,检验病人尿液中是否含有葡萄糖,故C正确;
D.二氧化硫和水反应生成亚硫酸,所以导致雨水的pH值小于5.6,亚硫酸易被空气中的氧气氧化生成硫酸,使溶液的pH值变得更小,故D错误;
故选C.
点评 本题考查知识点较多,难度不大,根据元素化合物的性质分析解答即可,注意正常雨水的pH值5.6.


科目:高中化学 来源: 题型:选择题
| A. | CH4和CH3(CH2)2CH3 | B. | CH3CH3和CH3CH2CH3 | ||
| C. | CH2=CH2和CH2=CHCH3 | D. | CH3(CH2)2CH3和CH3CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 钠是一种具有强还原性的金属,可用于冶炼钛、锆、铌等金属 | |
| C. | 晶体硅熔点高硬度大,可用于制作半导体材料 | |
| D. | 小苏打受热易分解,常用于做面包发酵粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子的还原性强弱:I->Fe2+>Cl- | |
| B. | 当a>b时,发生的离子反应:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 当a=b时,发生的离子反应:2I-+Cl2═I2+2Cl- | |
| D. | 当3a≤2b时,发生的离子反应:2Fe2++4I-+3Cl2═2Fe3++2I2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应中氧化剂是Na2O2,还原剂是FeSO4 | |
| B. | 生成2molNa2FeO4时,反应中共有8mol电子转移 | |
| C. | 反应中生成22.4LO2时,共有10mol电子转移 | |
| D. | Na2FeO4净水过程中,既有氧化还原反应发生,又有非氧化还原反应发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子.请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)
已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子.请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Cu、Ag分别作原电池两电极,AgNO3溶液作电解质溶液 | |
| B. | 用Ag作电解池的阳极,石墨作电解池的阴极,CuSO4溶液作电解质溶液 | |
| C. | 用Ag、C分别作原电池两电极,CuSO4溶液作电解质溶液 | |
| D. | 用Ag作电解池的阳极,石墨作电解池的阴极,AgNO3溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
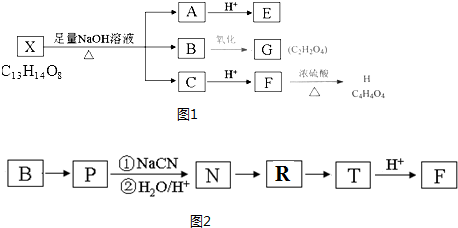
 +(2n-1)H2O.
+(2n-1)H2O.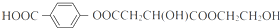 .
.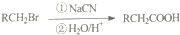
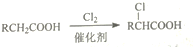

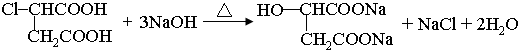 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com