
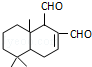
 某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )| A. | Br2的CCl4溶液 | B. | HBr | C. | Ag(NH3)2OH溶液 | D. | H2 |
分析 A.碳碳双键发生加成反应,醛基和溴发生氧化反应;
B.碳碳双键发生加成反应;
C.醛基和银氨溶液发生氧化反应生成羧基;
D.碳碳双键、醛基都发生加成反应.
解答 解:A.碳碳双键发生加成反应,醛基和溴发生氧化反应,所以增加溴原子,故A错误;
B.碳碳双键和HBr发生加成反应,官能团由碳碳双键变为溴原子,HBr和醛基不反应,所以官能团数目不变,故B错误;
C.醛基和银氨溶液发生氧化反应生成羧基,官能团数目不变,故C错误;
D.碳碳双键、醛基都发生加成反应,生成物只有羟基,官能团数目减少,故D正确.
故选D.
点评 本题考查了有机物的结构及性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物中含有的官能团及其性质,明确物质能发生哪些类型的反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 48gO3含有的氧原子数目为NA | |
| B. | 常温常压下,22.4L Cl2含有的分子数目为NA | |
| C. | 1molAl与足量氢氧化钠溶液完全反应时失去的电子数目为3NA | |
| D. | 1mol•L-1K2CO3溶液中含有的钾离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 所含离子 | Na+ | HCO3- | CO32- | SO32- | HSO3- |
| 浓度mol/L | 0.005 | 0.01 | 0.05 | 0.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol/L Na2CO3溶液:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | 1.0mol/L Na2CO3溶液:c(H2CO3)+c(HCO3-)+c(CO32-)+C(Na+)=3.0mol/L | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
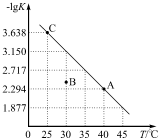 将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )| A. | 该反应的△H>0 | |
| B. | 30℃时,B点对应状态的v(正)<v(逆) | |
| C. | A点对应状态的平衡常数K(A)=10-2.294 | |
| D. | NH3的体积分数不变时,该反应一定达到平衡状态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com