
ÓĆŅ»ÖÖŅõ”¢ŃōĄė×ÓĖ«øōĤȿŹŅµē½ā²Ū“¦Ąķ·ĻĖ®ÖŠµÄNH4+£¬Ä£Äā×°ÖĆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
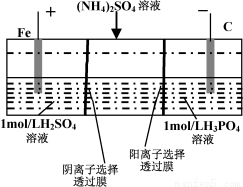
A£®Ńō¼«ŹŅČÜŅŗÓÉĪŽÉ«±ä³É×Ų»ĘÉ«
B£®Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ4OHØC-4eØC=2H2O+O2”ü
C£®µē½āŅ»¶ĪŹ±¼äŗó£¬Ņõ¼«ŹŅČÜŅŗÖŠµÄpHÉżøß
D£®µē½āŅ»¶ĪŹ±¼äŗó£¬Ņõ¼«ŹŅČÜŅŗÖŠµÄČÜÖŹŅ»¶ØŹĒ(NH4)3PO4

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ°²»ÕŹ””°½»“Ź®Š£”±øßČż4ŌĀĮŖæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹöŗĶĶĘĀŪ¶¼ÕżČ·µÄŹĒŠšŹö
ŠšŹö | ĶĘĀŪ | |
A | ĖįŠŌ£ŗHCl>H2CO3>H2SiO3 | ·Ē½šŹōŠŌ£ŗCl>C>Si |
B | ×é³ÉŌµē³ŲŹ±£¬Ķس£ŹĒ»¹ŌŠŌ½ĻĒæµÄĪļÖŹ×öøŗ¼« | Ć¾ŗĶĀĮŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ×é³ÉŌµē³ŲŹ±£¬Ć¾×öøŗ¼« |
C | ”ŖOHŹĒĒ×Ė®»ł£¬ŗ¬ÓŠ”ŖOHµÄÓŠ»śĪļ¶¼Ņ×ČÜÓŚĖ® | ³£ĪĀŹ±£¬C2H5OHŗĶ |
D | Čܽā¶ČŠ”µÄ³ĮµķæÉ×Ŗ»Æ³ÉČܽā¶ČøüŠ”µÄ³Įµķ | ĻņAgClµÄŠü×ĒŅŗÖŠµĪ¼ÓKIČÜŅŗæÉŅŌµĆµ½AgI³Įµķ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ½ĖÕŹ”Ģ©ÖŻŹŠøßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
“óĘųĪŪČ¾ŌŁ“Ī³ÉĪŖ½ńÄź”°Į½»į”±µÄČČĆÅŅéĢā”£ĻĀĮŠ×ö·Ø²»ÄÜøÄÉĘ“óĘų»·¾³µÄŹĒ
A£®“óĮ¦æŖ·¢ŠĀÄÜŌ“ŗĶæÉŌŁÉśÄÜŌ“
B£®³ĒŹŠ“óĮ¦·¢Õ¹¹ģµĄ½»ĶØ£¬ÉŁæŖĖ½¼Ņ³µ
C£®Ēå½ąČ¼Ćŗ”¢ĢįøßČ¼ÓĶĘ·ÖŹ
D£®Ń§Š£”¢¼ŅĶ„°²×°æÕĘų¾»»Æ×°ÖĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ½ĖÕŹ”ÄĻĶØ”¢ŃļÖŻ”¢Į¬ŌĘøŪøßČżµŚ¶ž“Īµ÷ŃŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®³£ĪĀ³£Ń¹ĻĀ£¬2.24 L H2OÖŠŗ¬ÓŠ¼«ŠŌ¹²¼Ū¼üµÄŹżÄæĪŖ0.2 NA
B£®0.1 mol”¤L£1 NH4ClČÜŅŗÖŠŗ¬ÓŠNH4£«µÄŹżÄæŠ”ÓŚ0.1 NA
C£®100 mL 12 mol”¤L£1µÄÅØHNO3Óė¹żĮæCu·“Ó¦×ŖŅʵē×ӵďżÄæĪŖ0.6 NA
D£®±ź×¼×“æöĻĀ£¬11.2 LÓÉCH4ŗĶC2H4×é³ÉµÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠĒāŌ×ӵďżÄæĪŖ2 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ¼ŖĮÖŹ”³¤“ŗŹŠøßČżÖŹĮæ¼ą²āČżĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
Ń”æ¼[»Æѧ”ŖŃ”ŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ]£Ø15·Ö£©ŃŖŗģµ°°×ŹĒøßµČÉśĪļĢåÄŚøŗŌšŌĖŌŲŃõµÄŅ»ÖÖµ°°×ÖŹ(ĖõŠ“ĪŖHB»ņHGB)”£ÓėÕż³£ŃŖŗģµ°°×Ļą±Č£¬ĮņŃŖŗģµ°°×²»ÄÜÓėŃõ³ŹæÉÄęµÄ½įŗĻ£¬Ņņ“ĖŹ§Č„ŠÆ“ųŃõµÄÄÜĮ¦”£ĻĀĶ¼ĖłŹ¾ĪŖĮņŃŖŗģµ°°×µÄ½į¹¹”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ĮņŃŖŗģµ°°×ÖŠĖłŗ¬·Ē½šŹōŌŖĖŲÖŠµēøŗŠŌ×ī“óŌŖĖŲŹĒ_____£¬µŚŅ»µēĄėÄÜ×ī“óµÄŌŖĖŲµÄŌ×ÓŹĒ__”£
£Ø2£©øł¾ŻµČµē×ÓĢåŌĄķĶʶĻŃõŌŖĖŲµÄŅ»ÖÖĶ¬ĖŲŅģŠĪĢåO3ŹĒ______·Ö×Ó(Ģī”°¼«ŠŌ”±»ņ”°·Ē¼«ŠŌ”±)”£ÅØĮņĖįÕ³¶Č½Ļ“óµÄŌŅņŹĒ___________”£
£Ø3£©ĮņŃŖŗģµ°°×ÖŠCŌ×ÓµÄŌӻƷ½Ź½ĪŖ__________”£ŌŚĶ¼ÖŠÓĆ”°”ś”±±ź³öNŗĶFe2+ŠĪ³ÉµÄÅäĪ»¼ü”£
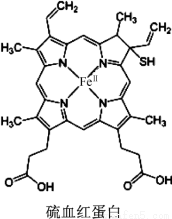
£Ø4£©ĢśµÄ½šŹōĆܶѻż·½Ź½ĪŖĢåŠÄĮ¢·½½į¹¹£¬½į¹¹ČēĶ¼ĖłŹ¾”£
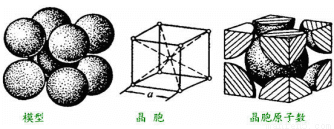
Ōņ¾§°ūÖŠĢśŌ×ÓµÄÅäĪ»ŹżĪŖ__________”£Čē¹ūĢśŌ×ӵİė¾¶ĪŖr pm£¬ĮŠŹ½²¢¼ĘĖć³öøƶѻż·½Ź½µÄæÕ¼äĄūÓĆĀŹ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ¼ŖĮÖŹ”³¤“ŗŹŠøßČżÖŹĮæ¼ą²āČżĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅģĪģĶéµÄ¶žĀČ“śĪļµÄĶ¬·ÖŅģ¹¹ĢåÓŠ
A£®6ÖÖ B£®8ÖÖ C£®10ÖÖ D£®12ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗžÄĻŹ”ŅęŃōŹŠøßČżĖÄŌĀµ÷ŃŠæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
£Ø13·Ö£©ŹµŃéŹŅĄūÓƱł“×ĖįŗĶÕż¶”“¼ÖʱøŅŅĖįÕż¶”õ„£¬ŹµŃé×°ÖĆČēĻĀĶ¼ĖłŹ¾£¬æÉÄÜÓƵ½µÄÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
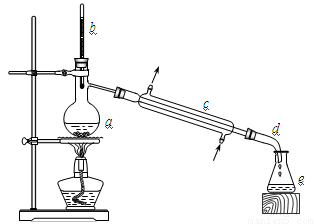
Õż¶”“¼ | ±ł“×Ėį | ŅŅĖįÕż¶”õ„ | Õż¶”ĆŃ | |
ĆܶČ/(g/cm3) | 0.810 | 1.049 | 0.882 | 0.7689 |
·Šµć/”ę | 118.0 | 118.1 | 126.1 | 142 |
ŗĻ³É·“Ó¦£ŗŌŚøÉŌļµÄaÖŠ¼ÓČė9.32 gÕż¶”“¼”¢7.2 mL ±ł“×ĖįŗĶ3”«4µĪÅØĮņĖį£¬Ņ”ŌČŗ󣬼ӼøĮ£·ŠŹÆ£¬cÖŠĶØĖ®£¬æŖŹ¼»ŗĀż¼ÓČČ£¬æŲÖĘĮó³öĪļµÄĪĀ¶Č²»³¬¹ż130”ę”£
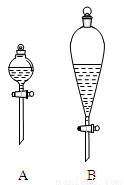
·ÖĄėĢį“æ£ŗ¢Ł½«ŅĒĘ÷aÖŠ·“Ó¦ŗóµÄ»ģŗĻŅŗÓėŅĒĘ÷eÖŠµÄĮó³öĪļŗĻ²¢£¬×ŖČė·ÖŅŗĀ©¶·ÖŠ£»¢ŚŅĄ“ĪÓĆĖ®”¢ÉŁĮæµÄ10%Ģ¼ĖįÄĘČÜŅŗŗĶĖ®Ļ“µÓ£¬·ÖĄėŗóŌŁ¼ÓøÉŌļ¼ĮM£¬¾²ÖĆŅ»¶ĪŹ±¼äŗó£¬ĘśČ„M£»¢Ū½«×īÖÕµĆµ½µÄ·“Ó¦“Ö²śĪļ×ŖČėĻ“¾»µÄŅĒĘ÷aÖŠ£¬¼ÓČė¼øĮ£·ŠŹÆ£¬½ųŠŠÕōĮó£¬µĆµ½ŅŅĖįÕż¶”õ„7.31 g”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅĒĘ÷aµÄĆū³ĘŹĒ_____________”£
£Ø2£©ŌŚ·ÖŅŗŹ±Ó¦Ń”ČēĶ¼×°ÖĆÖŠµÄ____£ØĢīŠņŗÅ£©£¬Ź¹ÓĆøĆŅĒĘ÷Ē°Ó¦ĻČ___”£
£Ø3£©Š“³öÖʱøŅŅĖįÕż¶”õ„µÄ»Æѧ·½³ĢŹ½£ŗ_______________________”£
£Ø4£©µŚŅ»“ĪĖ®Ļ“µÄÄæµÄŹĒ____________________________”£
£Ø5£©øÉŌļ¼ĮMæÉŅŌŹĒ_______£ØĢīŠņŗÅ£©
A£®ĪåŃõ»Æ¶žĮ× B£®ĪŽĖ®ĮņĖįÄĘ
C£®¼īŹÆ»Ņ D£®ĒāŃõ»ÆÄĘ¹ĢĢå
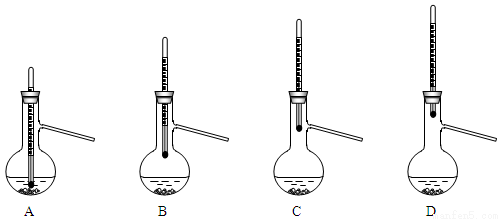
£Ø6£©²½Öč¢ŪµĆµ½µÄ“Ö²śĘ·ÕōĮóĢį“æŹ±£¬ĻĀĶ¼ĖłŹ¾×°ÖĆÖŠ£¬ĪĀ¶Č¼ĘĪ»ÖĆæÉÄܵ¼ÖĀŹÕ¼Æµ½µÄ²śĘ·ÖŠ»ģÓŠøß·ŠµćŌÓÖŹµÄ×°ÖĆĪŖ______£ØĢīŠņŗÅ£©
£Ø7£©±¾ŹµŃéĖłµĆµ½µÄŅŅĖįÕż¶”õ„µÄ²śĀŹŹĒ__________£ØĢīŠņŗÅ£©
A£®30% B£®40% C£®50% D£®55%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗžÄĻŹ”»³»ÆŹŠøßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
X”¢Y”¢Z”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲ£®ĘäÖŠÖ»ÓŠŅ»ÖÖŹĒ½šŹōŌŖĖŲ£¬X”¢WĶ¬Ö÷×åĒŅÄÜŠĪ³ÉŅ»ÖÖĄė×Ó»ÆŗĻĪļWX£»YµÄĘųĢ¬Ēā»ÆĪļ”¢×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļæÉ·“Ӧɜ³ÉŅ»ÖÖŃĪ£»ZŌ×ÓµÄ×īĶā²ćµē×ÓŹżÓėĘäµē×Ó×ÜŹżÖ®±ČĪŖ3©U4”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®Ō×Ó°ė¾¶£ŗW£¾Z£¾Y£¾X
B£®Ēā»ÆĪļĪČ¶ØŠŌ£ŗY£¾Z
C£®WY3ÖŠÖ»ÓŠĄė×Ó¼üƻӊ¹²¼Ū¼ü
D£®XÓėZæÉŠĪ³Él0µē×Ó·Ö×ÓŗĶ18µē×Ó·Ö×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğĢģ½ņŹŠŗĶĘ½ĒųøßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĶ¼ĪŖ³£ĪĀĻĀÓĆ0.10mol”¤L£1NaOHČÜŅŗµĪ¶Ø20.00 mL 0.10 mol”¤L£1ŃĪĖįŗĶ20.00 mL 0.10 mol”¤L£1“×ĖįµÄĒśĻß”£ČōŅŌHA±ķŹ¾Ėį£¬ĻĀĮŠÅŠ¶ĻŗĶĖµ·ØÕżČ·µÄŹĒ
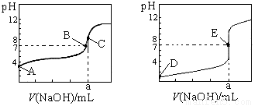
A£®×óĶ¼ŹĒµĪ¶ØŃĪĖįµÄĒśĻß
B£®EµćŹ±ČÜŅŗÖŠĄė×ÓÅضČĪŖc£ØNa+£©= c£ØA”Ŗ£©
C£®BµćŹ±£¬·“Ó¦ĻūŗÄČÜŅŗĢå»ż£ŗV£ØNaOH£©£¾V£ØHA£©
D£®µ±0mL£¼V£ØNaOH£©£¼20. 00mLŹ±£¬ČÜŅŗÖŠŅ»¶ØŹĒc£ØA££©£¾c£ØNa+£©£¾c£ØH+£© £¾c£ØOH££©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com