
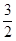 O2(g)====SO2(g)+H2O(L) △H=-akJ·mol-1(2分,其他答案合理也可给分)
O2(g)====SO2(g)+H2O(L) △H=-akJ·mol-1(2分,其他答案合理也可给分)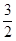 O2(g)====SO2(g)+H2O(L) △H=-akJ·mol-1;(4)ZX为NaH,其电子式为Na+[:H]-;ZX与水反应放出气体的化学方程式为:NaH+H2O====NaOH+H2↑。
O2(g)====SO2(g)+H2O(L) △H=-akJ·mol-1;(4)ZX为NaH,其电子式为Na+[:H]-;ZX与水反应放出气体的化学方程式为:NaH+H2O====NaOH+H2↑。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.②③④ |
| C.②③④⑤ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径A>B>D>C | B.原子序数d>c>b>a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.O、S、Na、K的原子半径依次增大 |
| B.Na、Mg、Al、Si的金属性逐渐增强 |
| C.钾离子氧化性比钠离子强 |
| D.Mg(OH)2、Al(OH)3、KOH、Ca(OH)2碱性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲原子电子层数比乙原子的电子层数多 |
| B.在甲乙两种金属和盐酸构成的原电池中,甲作正极,乙作负极 |
| C.1mol 甲和乙分别与足量的盐酸反应,产生H2的量:甲>乙 |
| D.常温时,甲能从水中置换出氢,而乙不能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.原子结构示意图为 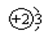 | B.原子核内中子数为3 |
| C.1mol 3He的质量约为3g | D.3He的摩尔质量为3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y原子中电子数较X原子多一个,但比Z原子少一个 |
| B.Y单质和Z、X的单质均可以反应 |
| C.元素Z为活泼的金属,其单质跟水反应放出氢气,生成物的水溶液显碱性 |
| D.X原子与氢反应能形成HX |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com