
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:名卷汇编(化学) 题型:013
用![]() 表示阿伏加德罗常数,下列说法是不正确的是
表示阿伏加德罗常数,下列说法是不正确的是
[ ]
A.常温常压下,活泼金属从盐酸中置换出1mol![]() ,发生转移的电子数为2
,发生转移的电子数为2![]()
B.醋酸的摩尔质量与![]() 个醋酸分子的质量在数值上相等
个醋酸分子的质量在数值上相等
C.标准状况下,22.4L氨气所含电子数为7![]()
D.a g某气体含分子数为b,则c
g该气体在标准状况下的体积为![]() L
L
查看答案和解析>>
科目:高中化学 来源:山东省泰安市2011届高三上学期期末考试化学试题 题型:013
|
NA代表阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
1 L 1 mol·L-1的Na2SO4溶液中含有Na+的个数为NA |
B. |
2 g氢气所含氢原子数目为NA |
C. |
在常温常压下,11.2 L氮气所含的原子数目为NA |
D. |
1.7 g氨气所含分子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市闵行区高三下学期三模考试化学试卷(解析版) 题型:填空题
2013年初,雾霾天气多次肆虐我国中东部,该地区PM2.5严重超标。研究表明,PM2.5约60%来源于某些气体污染物在空气中转变而成的二次颗粒物。这些气体污染物主要有二氧化硫、氮氧化物、氨气、挥发性有机物。因此,控制、治理PM2.5污染源成为环保的重要课题。
(1)研究表明,TiO2在紫外线照射下会使空气中的某些分子产生活性基团OH,如图所示,OH与NO2的反应为NO2+OH HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是
。
HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是
。
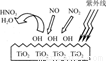
(2)如图所示的电解装置能吸收和转化NO2、NO和SO2。阴极排出的溶液中含S2O42-离子,能吸收NOx气体,生成的SO32-可在阴极区再生。请将S2O42-吸收NO2的离子方程式配平,并标明电子转移的方向和数目。
____S2O42-+____NO2+____OH- SO32-+____N2+____
SO32-+____N2+____
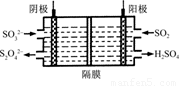
(3)已知上述电解装置阳极反应为:SO2-2e-+2H2O SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为
。
SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为
。
(4)PM2.5产生的主要来源是日常发电、工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自扬尘等;2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(如机动车尾气、燃煤)、挥发性有机物的排放等。请你结合信息,给出降低PM2.5排放的对策(至少两条): ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com