
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 900 | a | b | c | d | t |
分析 (1)CO(g)+H2O(g)?CO2(g)+H2(g),反应的平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;平衡常数随温度升高减小,说明升温平衡逆向进行;若改变条件使平衡向正反应方向移动,平衡常数不一定变化,平衡常数只随温度变化;
(2)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)①实验A中CO的转化率为$\frac{4mol-2.4mol}{4mol}$×100%=40%,实验B中CO的转化率为$\frac{2mol-1.6mol}{2mol}$×100%=20%,利用转化率与消耗量和起始量的关系计算并判断反应热;
②从等效平衡的角度分析,若实验C要达到与实验B等效的平衡状态,则所加入物质的物质的量之比等于初始原料的配比数.
解答 解:(1)CO(g)+H2O(g)?CO2(g)+H2(g),K=$\frac{{(CO)•({H_2})}}{{(CO)•({H_2}O)}}$,平衡常数随温度升高减小,说明升温平衡逆向进行,逆反应为吸热反应,正反应为放热反应,若改变条件使平衡向正反应方向移动,则平衡常数不一定变化,平衡常数只随温度变化,浓度变化不影响平衡常数,则平衡向正反应方向移动可能增大,
故答案为:$\frac{{(CO)•({H_2})}}{{(CO)•({H_2}O)}}$; 放热;③;
(2)a、容器中压强始终不变,不能说明反应达到平衡状态,故a错误;
b、混合气体中c(CO)不变,是平衡的标志,故b正确;
c、v正(H2)=v正(H2O)=v逆(H2O),正逆反应速率相等,但不为0,能说明反应达到平衡状态,故c正确;
d、c(CO2)=c(CO)可能是平衡状态,也可能不是,与各物质的初始浓度及转化率有关,故d错误;
故答案为:b c;
(3)①实验A中CO的转化率为$\frac{4mol-2.4mol}{4mol}$×100%=40%,实验B中CO的转化率为$\frac{2mol-1.6mol}{2mol}$×100%=20%,则实验A的转化率大于实验B,
则说明温度升高平衡向逆反应方向移动,该反应放热,故答案为:大于;放;
②若实验C要达到与实验B等效的平衡状态,则所加入物质的物质的量之比等于初始原料的配比数,即b=2a,故答案为:b=2a.
点评 本题考查化学平衡常数的应用、化学平衡移动,等效平衡的分析判断,掌握化学平衡常数的书写与应用和平衡移动原理是解题关键,题目难度中等.


科目:高中化学 来源: 题型:实验题
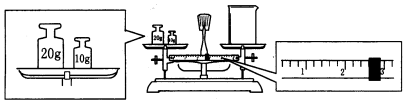
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,1L pH=13的氢氧化钡溶液所含OH- 数为0.2NA | |
| B. | 标准状况下,0.1molAl3+含有的核外电子数为0.3 NA | |
| C. | 常温下,44gCO2中含有2NA个碳氧双键 | |
| D. | 将1 molN2 和3mol H2 通入密闭容器中,一定条件下充分反应,转移电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O=2 NaOH+H2↑ | B. | Cl2+H2O=HCl+HClO | ||
| C. | CaCO3=CaO+CO2↑ | D. | Ca(ClO)2+2HCl=CaCl2+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
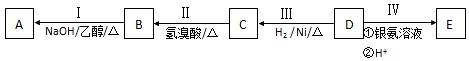
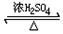 (CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O;
(CH3)2CHCH2COOCH2CH2CH(CH3)2+H2O; 和
和 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 醋酸钠中加入盐酸:CH3COONa+H+→CH3COOH+Na+ | |
| B. | 在硫酸作催化剂、加热条件下乙烯与水发生加成反应:CH2═CH2+H2O $→_{△}^{H_{2}SO_{4}}$ CH3CH2OH | |
| C. | 甲醛溶液中加入足量的银氨溶液并加热: HCHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$HCOO-+NH4++2Ag↓+3NH3+H2O | |
| D. | 2分子甘氨酸 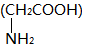 在一定条件下脱去2分子水: 在一定条件下脱去2分子水: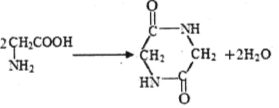 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com