
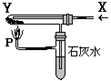
| A.H2和NaHCO3(白) | B.CO2和Na2O2(黄); |
| C.CO和Cu2(OH)2CO3(绿) | D.CO和Fe2O3(红); |
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源:不详 题型:填空题
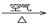 CuO
CuO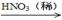 Cu(NO3)2
Cu(NO3)2 | A.40.32L | B.30.24L | C.20.16L | D.13.44L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
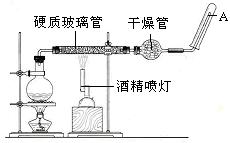
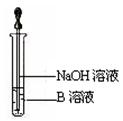
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 加硫酸的序号 | 每次加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 16.0 |
| 2 | 20.0 | 12.0 |
| 3 | 20.0 | 8.0 |
| 4 | 20.0 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.称取15.2g硫酸铜固体,加入1000 mL水 |
B.称取2 4g胆矾溶于水配成1000 mL溶液 4g胆矾溶于水配成1000 mL溶液 |
| C.称取16 g硫酸铜固体,加入1000 mL水 |
| D.称取25 g胆矾溶于水配成1000 mL溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 O的质量之比。
O的质量之比。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com