
如下图,瓶a内放入20mL6mol/L盐酸,b是未充气的气球,里面放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口上,并用弹簧夹d夹紧(瓶口和侧口都不漏气).将图(Ⅰ)的装置在天平上称量,质量为W1 g.根据实验现象填写下列空白:
(1) 把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ).反应结束后,再次称量,质量为W2
g. 则![]() 和
和![]() 的关系是________.
的关系是________.
(2) 取25mL6mol/L NaOH溶液,先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气),打开d,将溶液挤入瓶中,立即夹紧d,可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失.使沉淀消失的反应的化学方程式是________.
(3) 将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量沉淀,不再溶解,此时瓶内温度________(填“不变”、“降低”或“升高”).
(4) 继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状.写出这时发生的反应的化学方程式________.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
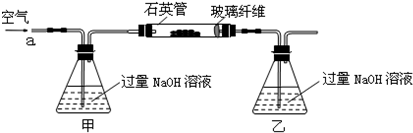
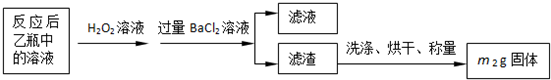
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 24.97 |
查看答案和解析>>
科目:高中化学 来源: 题型:058
如下图所示,图(Ⅰ)中瓶a内放入20 mL 6 mol/L盐酸,b是未充气的气球,里边放有4 g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气).
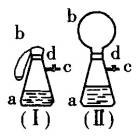
将图(Ⅰ)的装置放在托盘天平上称量,质量为![]() g.根据实验现象填写下列空白:
g.根据实验现象填写下列空白:
(1)把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ).反应结束后,再次称量,质量为![]() .则
.则![]() 和
和![]() 的关系是_____________.
的关系是_____________.
(2)取25 mL6 mol/LNaOH溶液,先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气).打开d,将溶液挤入瓶中,立即夹紧d.可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失.使沉淀消失的反应的化学方程式是____________________.
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解.此时瓶内温度_____________(填“不变”、“降低”或“升高”).
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状.写出这时发生的反应的化学方程式_____________.
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
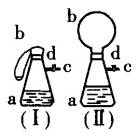
将图(Ⅰ)的装置放在托盘天平上称量,质量为![]() g.根据实验现象填写下列空白:
g.根据实验现象填写下列空白:
(1)把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ).反应结束后,再次称量,质量为![]() .则
.则![]() 和
和![]() 的关系是_____________.
的关系是_____________.
(2)取25 mL6 mol/LNaOH溶液,先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气).打开d,将溶液挤入瓶中,立即夹紧d.可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失.使沉淀消失的反应的化学方程式是____________________.
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解.此时瓶内温度_____________(填“不变”、“降低”或“升高”).
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状.写出这时发生的反应的化学方程式_____________.
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江西省南昌市高三第三次模拟测试理综化学部分 题型:实验题
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对某黄铁矿石(主要成 分为FeS2)进行硫元素含量测定的实验探究及工业生产硫酸的探究.
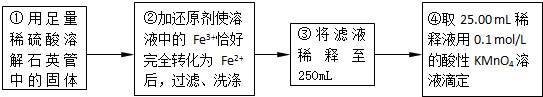
I.将m1g该黄铁矿样品(杂质中不含硫和铁)放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通人空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:4FeS2+11O2→2 Fe2O3+8SO2(高温)

Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:

问题讨论:
(1)1中,甲瓶内所盛试剂是 溶液。乙瓶内发生反应的离子方程式有
、 。
(2)Ⅱ中,所加H2O2溶液需足量的理由是 。
(3)该黄铁矿石中硫元素的质量分数为 。
(4)在硫酸工业中,通过下列反应使二氧化硫转化为三氧化硫:
 在实际工业生产中,常采用“二转 二吸法”,即将第一次转化生成的SO2分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为 。
在实际工业生产中,常采用“二转 二吸法”,即将第一次转化生成的SO2分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为 。
(5)硫酸的工业制法过程涉及三个主要的化学反应及相应的设备(沸腾炉、转化器、吸收塔)。
①三个设备分别使反应物之间或冷热气体间进行了“对流”。请简单描述吸收塔中反应物之间是怎样对流的 。
②工业生产中常用氨一酸法进行尾气脱硫,以达到消除污染、废物利用的目的,用化学方程式表示其反应原理。(只写出2个方程式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com