
 HCO3-+OH-,下列说法正确的是( )
HCO3-+OH-,下列说法正确的是( ) | A.稀释溶液,水解平衡常数增大 |
| B.加入NaOH固体,c(HCO3-)/c(CO32-) 减少 |
| C.升高温度,平衡常数减小 |
| D.通入CO2,pH增大 |
科目:高中化学 来源:不详 题型:单选题
| A.绝对不溶解的物质是不存在的 |
| B.不溶于水的物质溶解度为0 |
| C.物质的溶解性为难溶,则该物质不溶于水 |
| D.某离子被沉淀完全是指该离子在溶液中的浓度为0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.白色沉淀为ZnS,黑色沉淀为CuS |
| B.利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| C.上述现象说明ZnS的Ksp小于CuS的Ksp |
| D.该过程破坏了ZnS的溶解平衡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 相关化合物 | AgX | AgY | AgZ |
| pKsp | a | b | c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
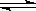 Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是| A.加入少量MgCl2固体 | B.加入少量Na2CO3固体 |
| C.加入少量KCl固体 | D.加入少量Ba(OH)2固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.温度升高,Ksp(AgCl)不变 |
| B.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大 |
| C.常温下,将0.001 mol?L-1 AgNO3溶液滴入0.001 mol·L-1 KCl和 0.001 mol·L-1 K2CrO4溶液先产生Ag2CrO4沉淀 |
| D.在Mg 2+为0.12 mol?L-1的溶液中要产生Mg(OH)2沉淀,应控制溶液的pH>9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.温度一定时,Ksp(SrSO4)随c(SO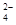 )的增大而减小 )的增大而减小 |
| B.三个不同温度中,313 K时Ksp(SrSO4)最大 |
| C.283 K时,图中a点对应的溶液是饱和溶液 |
| D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgCl=AgI=Ag2S | B.AgCl<AgI<Ag2S |
| C.AgCl>AgI>Ag2S | D.AgI>AgCl>Ag2S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.5×10-16 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com