
【题目】SO2的含量是衡量大气污染的一个重要指标,工业上常采用催化还原法或吸收法处理SO2。利用催化还原SO2不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和H2O。
己知CH4和S的燃烧热(△H)分别为-890.3 kJ /mol和-297.2 kJ /mol,则CH4和SO2反应的热化学方程式为 _________________________________________________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:
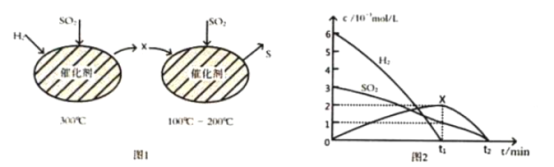
①分析可知X为________(写化学式), 0~t1时间段的温度为_____, 0~t1时间段用SO2表示的化学反应速率为 ___________________________。
②总反应的化学方程式为__________________________________________________________。
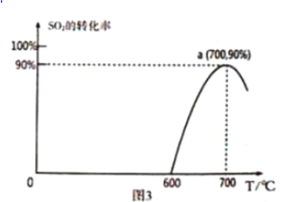
(3)焦炭催化还原SO2生成S2,化学方程式为:2C(s)+2SO2(g)![]() S2(g)+2CO2(g),恒容容器中,1 mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
S2(g)+2CO2(g),恒容容器中,1 mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
①该反应的△H _________________________ 0 (填“>”或“<”)
②计算700℃该反应的平衡常数为____________________ 。
【答案】CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) △H=-295.9kJ/mol H2S 300℃ 2×10-3/t1mol/(Lmin) 2H2+SO2![]() S+2H2O < 36.45mol/L
S+2H2O < 36.45mol/L
【解析】
(1)CH4的燃烧的热化学反应方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1 ①,S燃烧的热化学反应方程式为S(s)+O2(g)=SO2(g) △H=-297.2kJ·mol-1 ②,CH4和SO2反应的方程式为CH4+2SO2=2S+CO2+2H2O,
因此有①-2×②得出CH4(g)+SO2(g)=2S(s)+CO2(g)+2H2O(l) △H=(-890.3+2×297.2)kJ·mol-1=-295.9kJ·mol-1;
(2)①H2还原SO2发生反应:2H2+SO2=S+2H2O,图1右侧,SO2→S,S元素的化合价降低,根据氧化还原反应特点,化合价有升高,必然有降低,因此推出X为H2S;0~t1时间,X的浓度达到最大,应是图1左侧反应,4H2+SO2=H2S+2H2O,温度应为300℃;根据化学反应速率的表达式,v(SO2)=(3-1)/t1mol/(L·min);
②根据上述分析,总反应的化学方程式为2H2+SO2![]() S+2H2O;
S+2H2O;
(3)①根据图像,700℃SO2的转化率达到最大,反应达到平衡,右侧随着温度的升高,SO2的转化率降低,根据勒夏特列原理,正反应为放热反应,即△H<0;
②2C(s)+2SO2(g)![]() S2(g)+2CO2(g)
S2(g)+2CO2(g)
起始: 1 0 0
变化: 0.9 0.45 0.9
平衡: 0.1 0.45 0.9 化学平衡常数的表达式为K=[c(S2)×c2(CO2)]/c2(SO2),代入数值,得出K=36.45。


科目:高中化学 来源: 题型:
【题目】现有一份澄清溶液, 可能含有 Na+、 K+、 NH4+、 Ca2+、 Fe3+、 SO42-、 CO32-、 SO32-、 Cl-、I-中的若干种, 且离子的物质的量浓度均为 0.1 mol·L-1(不考虑水解和水的电离)。 往该溶液中加入过量的盐酸酸化的 BaCl2 溶液, 无沉淀生成。 另取少量原溶液, 设计并完成如下实验:

则关于原溶液的判断中不正确的是
A. 是否存在 Na+、K+需要通过焰色反应来确定
B. 通过CCl4 层的颜色变化,也能判断出原溶液中是否存在Fe3+
C. 虽然实验过程引入了氯元素, 但不影响原溶液是否存在Cl-的判断
D. 肯定不存在的离子是 Ca2+、Fe3+、SO42-、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列转化关系中,烃A为石油的裂解气里含是较高的气体(碳元素的质量分数为0.857),B分子中含有三元环,分子式为C2H4O;1molD与足量Zn反应生成22.4LH2(标准状况);E为六元环化合物。请回答下列问题:

(1)写出A 的结构简式____________。
(2)①的反应类型为___________。
(3)D物质中含氧原子团的名称为___________;写出HOCH2CH2OH与金属钠反应的化学方程式___________。
(4)写出反应②的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Zn+NH4NO3+2HNO3 =Zn(NO3)2+N2↑+3H2O的反应中,参加反应的锌和被还原的硝酸根的物质的量之比是( )
A.1∶3B.1∶1C.1∶2D.3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应aA+bB![]() cC中,5分钟时分别测得在不同温度下物质的含量A%和C%,绘制变化曲线如图所示,下列说法正确的是( )
cC中,5分钟时分别测得在不同温度下物质的含量A%和C%,绘制变化曲线如图所示,下列说法正确的是( )

A. 该反应在T1、T3温度时达到过化学平衡
B. 该反应在T2温度时达到过化学平衡
C. 该反应的逆反应是放热反应
D. 升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质转化关系的说法中不正确的是

A. 图1中甲可能是Fe,X可能是Cl2
B. 图2中A可能为F2,C可能为O2
C. 图2中A可能为Ca(OH)2,C可能为NaOH
D. 图3中a可能为C,b可能为CO,c可能为CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z的原子序数依次增大,在周期表中Y分别与X、Z相邻。回答下列问题:
(1)若X、Y和Z的单质都为金属,Y与Z左右相邻,Z的单质被称为“国防金属”。则Y的单质在O2中燃烧产物中含有的化学键为____________________________。
(2)若X、Y和Z位于同一周期,高纯度Y单质常用于制造太阳能电池。则除去Y的氧化物中所含X氧化物杂质的方法是________________过滤、洗涤、干燥。
(3)若X原子最外层电子数是电子层数的2倍,Z与Y同主族,则X、Y、Z的简单气态氢化物中,沸点最高的是________________。(填化学式)
(4)若Y的原子序数等于X的2倍,T是Z的气态氢化物。
①写出Z2X对应的水化物分子的电子式________________。
②M是短周期中原子半径最大的元素,由M、X、Y元素组成的一种化合物与T的水溶液反应产生刺激性气味的气体,溶液变浑浊。写出反应的离子方程式:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com