


分析 (1)A.蓄电池点亮灯泡,属于电能转化为光能;
B.植物的光合作用属于太阳能转化为化学能;
C.高温下分解碳酸钙,热能转化为化学能;
(2)过氧化钠属于离子化合物,是由钠离子和过氧根离子构成的,钠离子和过氧根离子之间存在离子键、O-O原子之间存在非极性共价键;
(3)钙原子和氯原子通过得失电子形成氯化钙;
(4)元素的非金属性越强,其最高价氧化物的水化物酸性越强;氢化物中熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高;
(5)Se原子有5个电子层、最外层电子数是6,所以位于第5周期第VIA族,具有氧族元素性质,
A.氧族元素单质随着原子序数增大,其状态由气态转化为固态;
B.其最高价氧化物的水化物属于酸性氧化物,能和碱反应;
C.同一主族元素氢化物结构相似;
D.氧族元素除了O元素外,其氧化物都两种.
解答 解:(1)A.蓄电池点亮灯泡,该过程中,电能转化为光能、热能;
B.植物的光合作用是将太阳能转化为有机物,属于太阳能转化为化学能;
C.高温下分解碳酸钙,碳酸钙吸收能量而分解,所以属于热能转化为化学能;
故答案为:电能转化光能或热能;光能转化为化学能;热能转化为化学能;
(2)过氧化钠属于离子化合物,是由钠离子和过氧根离子构成的,钠离子和过氧根离子之间存在离子键、O-O原子之间存在非极性共价键,电子式为 ,故答案为:
,故答案为: ;
;
(3)钙原子和氯原子通过得失电子形成氯化钙,其形成过程为 ,故答案为:
,故答案为: ;
;
(4)元素的非金属性越强,其最高价氧化物的水化物酸性越强;氢化物中熔沸点与其相对分子质量成正比,但含有氢键的物质熔沸点较高,非金属性P>As,所以酸性H3AsO4<H3PO4,HF中含有氢键、HCl中不含氢键,所以熔沸点HF>HCl,故答案为:<;>;
(5)Se原子有5个电子层、最外层电子数是6,所以位于第5周期第VIA族,属于氧族元素,
A.氧族元素单质随着原子序数增大,其状态由气态转化为固态,S都是固体,且Se原子序数大于S,则Se单质为固体,故A错误;
B.其最高价氧化物的水化物属于酸性氧化物,能和碱反应,所以Se最高价氧化物的水化物能和NaOH发生反应,故B正确;
C.同一主族元素氢化物结构相似,所以其氢化物化学式为H2Se,故C正确;
D.氧族元素除了O元素外,其氧化物都两种,所以Se的氧化物有两种,故D错误;
故答案为:VIA;BC.
点评 本题考查较综合,涉及能量转化方式、电子式、同一主族元素性质递变规律等知识点,明确物质结构、物质性质即可解答,难点是过氧化钠电子式的书写方法.


科目:高中化学 来源: 题型:选择题
| A. | SO${\;}_{3}^{2-}$ | B. | CH3COO- | C. | Fe2+ | D. | Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
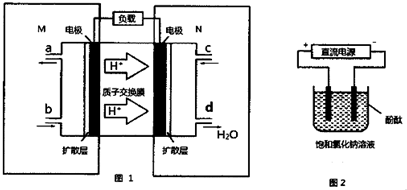
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
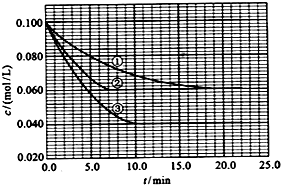 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
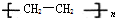 (塑料)、
(塑料)、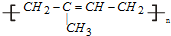 (橡胶).
(橡胶).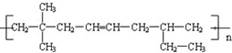 的单体为CH2=C(CH3)2、CH2=CH-CH=CH2、CH2=CHCH2CH3.
的单体为CH2=C(CH3)2、CH2=CH-CH=CH2、CH2=CHCH2CH3. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯和水、酒精和水、苯酚和水 | |
| B. | 二溴乙烷和水、溴苯和水、硝基苯和水 | |
| C. | 甘油和水、乙醛和水、乙酸和乙醇 | |
| D. | 油酸和水、甲苯和水、己烷和苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: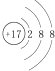 | |
| B. | 6个质子8个中子的碳元素的核素符号:12C | |
| C. | 氯化镁的电子式:[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]-Mg2+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| D. | 用电子式表示氯化氢的形成过程:H•+•$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$→H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com