
下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)===CO2(g) △H1 C(s)+ O2(g)===CO(g) △H2
O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+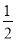 O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
A.① B.②③④ C.④ D.①②③
科目:高中化学 来源:2016届山东省高三上学期第一次检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.摩尔是用来衡量微观粒子多少的一种物理量
B.在一定的温度和压强下,各种气体的摩尔体积相等
C.阿伏加德罗常数的数值是0.012 kg 14C所含的原子个数
D.若气体摩尔体积为22.4 L•mol﹣1,则所处条件为标准状况
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上段中考试化学试卷(解析版) 题型:选择题
500ml 2mol/L的MgCl2溶液中含有氯离子的物质的量是
A.1 mol B.2 mol C.3 mol D.1000 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次月考化学试卷(解析版) 题型:填空题
(1)相同物质的量的CO2和O2,其分子数之比为 ,原子数之比为 ,氧原子数之比为 ;质量相同的CO2和O2,其物质的量之比为 。
(2)下列物质属于氧化物的是 (填序号,下同),属于碱的是 ,属于酸的是 ,属于盐的是 。其中⑥属于 (填“纯净物”或混合物)。①H2O ②NaCl ③H2SO4 ④Ca(OH)2 ⑤Fe3O4 ⑥CuSO4·5H2O ⑦HNO3 ⑧AgNO3 ⑨NaHCO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古奋斗中学高二上9月质检化学试卷(解析版) 题型:选择题
化学反应N2+3H2 2NH3的能量变化下图所示,该反应的热化学方程式是
2NH3的能量变化下图所示,该反应的热化学方程式是

A.N2(g)+3H2(g)  2NH3(1);△H=2(a-b-c)kJ·mol-1
2NH3(1);△H=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)  2NH3(g);△H=2(b-a)kJ·mol-1
2NH3(g);△H=2(b-a)kJ·mol-1
C.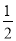 N2(g)+
N2(g)+ 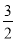 H2(g)
H2(g)  NH3(1);△H=(b+c-a)kJ·mol-1
NH3(1);△H=(b+c-a)kJ·mol-1
D.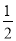 N2(g)+
N2(g)+ 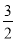 H2(g)
H2(g)  NH3(g);△H=(a+b)kJ·mol-1
NH3(g);△H=(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古奋斗中学高一上9月质检化学试卷(解析版) 题型:实验题
用18 mol·L-1 浓硫酸配制100 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④ ⑤转移、洗涤 ⑥定容、摇匀 ⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是 。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中_______________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水___________________;
C.所用过的烧杯、玻璃棒未洗涤___________________;
D.定容时俯视刻度线___________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古奋斗中学高一上9月质检化学试卷(解析版) 题型:选择题
在化学学科中,经常使用下列物理量,其中跟阿伏加德罗常数(NA)均无关的组合是
①摩尔质量(M)②相对原子质量(Mr)③物质的量(n)④原子半径(r)⑤溶质的质量分数(W)⑥溶解度(S)⑦气体摩尔体积(Vm)
A.①③⑥⑦ B.②④⑤⑥ C.①②③⑤ D.②③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:实验题
(14分)过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2)。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。

实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:
假设1:反应后固体中只有Na2SO3,证明SO2未被氧化;
假设2:反应后固体中只有 Na2SO4,证明SO2完全被氧化;
假设3: ,证明 。
实验探究:
实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
(2)试剂A可以选用____________________,试剂B的作用是________________________。
(3)实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g,装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据判断SO2未被氧化、完全被氧化的V-m1关系式。
未被氧化:____________________,完全被氧化:_______________________。
(4)若SO2完全被氧化,写出 反应的化学方程式: __________________________。
反应的化学方程式: __________________________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期中测试化学试卷(解析版) 题型:选择题
在373K 时,把0.5 mol N2O4气体通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol/L。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是
A.前2 s,以N2O4浓度变化表示的平均反应速率为0.01 mol·L-1·s-1
B.在2 s时,体系内压强为反应前的1.1倍
C.平衡时,体系内含N2O4 0.25 mol
D.平衡时,若往容器内充入氮气,则可提高N2O4的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com