
| AӢCu2+ӢSO42-ӢBa2+ӢCl- |
| BӢCa2+ӢNa+ӢNO3-ӢCO32- |
| CӢCl-ӢH+ӢNa+ӢCO32- |
| DӢNa+ӢNO3-ӢK+ӢSO42- |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| t/min | COmol/L£© | H2O£Ømol/L£© | CO2£Ømol/L£© | H2£Ømol/L£© |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.1 |
| 3 | n1 | n2 | n3 | 0.1 |
| 4 | 0.09 | 0.19 | 0.11 | 0.11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢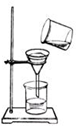 ¹żĀĖ |
B”¢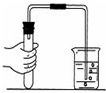 ¼ģ²é×°ÖƵÄĘųĆÜŠŌ |
C”¢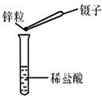 ½šŹōÓėĖį·“Ó¦ |
D”¢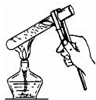 ¼ÓČČŅŗĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¢Ł¢Ś¢Ū | B”¢¢Ū¢Ü¢Ž |
| C”¢¢Ł¢Ū¢Ż | D”¢¢Ł¢Ū¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢æɽ«Éś»īĄ¬»ų·ŁÉÕ·¢µē£¬ŹµĻÖ׏Ō“»Æ“¦Ąķ |
| B”¢¶ŌĄ¬»ų·ÖĄą“¦ĄķŹĒĪŖĮĖŹ¹Ą¬»ųÖŠµÄŌŁÉś×ŹŌ“µĆµ½³ä·ÖĄūÓĆ |
| C”¢ĖłÓŠĄ¬»ųÖ»ŠčĶŚæÓ£¬Ēćµ¹£¬ÉīĀń¼“æÉ |
| D”¢Ą¬»ų“¦ĄķµÄ³£ÓĆ·½·ØÓŠĪĄÉśĢīĀń£¬¶Ń·ŹŗĶ·ŁÉÕµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| AӢ1 | BӢ2 | CӢ3 | DӢ4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢µČÓŚ1.06g |
| B”¢“óÓŚ1.06g£¬Š”ÓŚ2.86g |
| C”¢µČÓŚ2.86g |
| D”¢“óÓŚ2.86g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| c(O2)c(Hb?CO) |
| c(CO)c(Hb?O2) |
| c(Hb?CO) |
| c(Hb?O2) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Čō°ŃøĆ·“Ó¦Éč¼ĘĪŖŌµē³Ų£¬ŌņÕż¼«·“Ó¦ĪŖFe2+-e-=Fe3+ |
| B”¢Ńõ»Æ²śĪļĪŖNH4+ |
| C”¢Čō×ŖŅĘ5mole-ÓŠ1 mol NO3-±»»¹Ō |
| D”¢Ńõ»Æ¼ĮÓė»¹Ō¼ĮĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ8 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com