
| A | B | |
| C | D |

| »Æѧ¼ü | H-H | Br-Br | H-Br |
| ¼üÄÜ£ØkJ/mol£© | 436 | 194 | 362 |
| »ÆѧŹ½ | Ag2SO4 | AgBr |
| Čܽā¶Č£Øg£© | 0.796 | 8.4”Į10-6 |
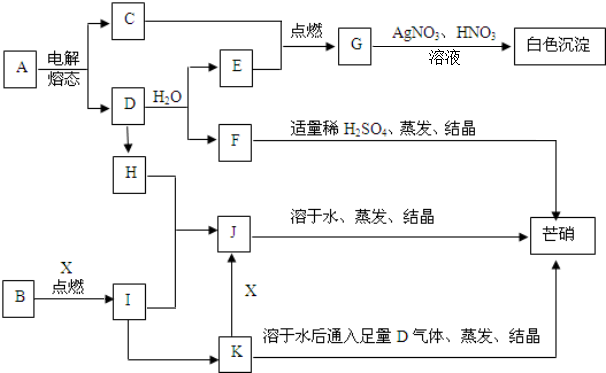
·ÖĪö ÓɶĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢DŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬A”¢B“¦ÓŚµŚ¶žÖÜĘŚ£¬C”¢D“¦ÓŚµŚČżÖÜĘŚ£¬B”¢D×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ12£¬¶žÕßĶ¬Ö÷×壬¹Ź×īĶā²ćµē×ÓŹżĪŖ6£¬ŌņBĪŖOŌŖĖŲ£¬DĪŖSŌŖĖŲ£¬¶žÕßæÉŅŌŠĪ³ÉSO2”¢SO3Į½ÖÖ·Ö×Ó£¬ĒŅSO2¾ßÓŠĘư׊Ō£¬ÓÉĪ»ÖĆ¹ŲĻµæÉÖŖ£¬AĪŖNŌŖĖŲ£¬CĪŖSiŌŖĖŲ£®
£Ø1£©Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀ·Ē½šŹōŠŌ¼õČõ£¬µ„ÖŹÓėĒāĘų·“Ó¦¾ēĮŅ³Ģ¶Č¼õŠ”£¬·“Ó¦ČČŌö“ó£Øæ¼ĀĒ·ūŗÅ£©£»
£Ø2£©¢ŁÓɹ¤ŅÕĮ÷³ĢĶ¼æÉÖŖ£¬µē½ā²ŪÖŠµē½āHBr£¬Éś³ÉH2ÓėBr2£¬øł¾Ż·“Ó¦ČČ=·“Ó¦Īļ×ܼüÄÜ-Éś³ÉĪļ×ܼüÄÜ£¬¼ĘĖćøĆ·“Ó¦µÄ·“Ó¦ČČ£¬¾Ż“ĖÉś³ÉČČ»Æѧ·½³ĢŹ½£»
¢Ś·ÖĄėĶźČ«£¬ĮņĖįÖŠ²»ŗ¬HBr£»
¢ŪŌŚŌµē³ŲÖŠ£¬øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬SO2ŌŚøŗ¼«·ÅµēÉś³ÉH2SO4£»
¢ÜŌŚµē½ā¹ż³ĢÖŠ£¬µē½ā²ŪŅõ¼«·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ2H++2e-=H2”ü£¬ĒāĄė×ÓÅØ¶Č½µµĶ£»
¢ŻŌµē³ŲÖŠµē³Ų×Ü·“Ó¦ĪŖSO2+Br2+2H2O=H2SO4+2HBr£¬µē½ā³ŲÖŠ×Ü·“Ó¦ĪŖ2HBr=H2+Br2£¬Į½Ź½Ļą¼ÓæɵĆøĆ¹¤ŅÕĮ÷³ĢÓĆ×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬
øĆÉś²ś¹¤ŅÕµÄÓŵć£ŗäåæÉŅŌŃ»·ĄūÓĆ£¬»ńµĆĒå½ąÄÜŌ“ĒāĘų£¬Č±µćŹĒ£ŗÉś³É¹ż³ĢÓŠÓŠ¶¾ĪļÖŹ£¬µē½āŃ»·ÄÜŌ““ó£»
£Ø3£©ŗ£Ė®Ģįäå¹ż³ĢÖŠ£¬ĻņÅØĖõµÄŗ£Ė®ÖŠĶØČėĀČĘų£¬½«ĘäÖŠµÄBr-Ńõ»Æ£¬ŌŁÓĆæÕĘų“µ³öäå£»Č»ŗóÓĆĢ¼ĖįÄĘČÜŅŗĪüŹÕä壬äåĘē»ÆĪŖBr-ŗĶBrO3-£¬Ķ¬Ź±Éś³ÉHCO3-»ņCO2£®
½ā“š ½ā£ŗÓɶĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢DŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬A”¢B“¦ÓŚµŚ¶žÖÜĘŚ£¬C”¢D“¦ÓŚµŚČżÖÜĘŚ£¬B”¢DĶ¬ÖÖÖ÷×壬B”¢D×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ12£¬¹Ź×īĶā²ćµē×ÓŹżĪŖ6£¬¹ŹBĪŖOŌŖĖŲ£¬DĪŖSŌŖĖŲ£¬¶žÕßæÉŅŌŠĪ³ÉSO2”¢SO3Į½ÖÖ·Ö×Ó£¬ĒŅSO2¾ßÓŠĘư׊Ō£¬ÓÉĪ»ÖĆ¹ŲĻµæÉÖŖ£¬AĪŖNŌŖĖŲ£¬CĪŖSiŌŖĖŲ£¬
£Ø1£©SeÓėOŌŖĖŲĶ¬×åŌŖĖŲ£¬Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀ·Ē½šŹōŠŌ¼õČõ£¬µ„ÖŹÓėĒāĘų·“Ó¦¾ēĮŅ³Ģ¶Č¼õŠ”£¬·“Ó¦ČČŌö“ó£Øæ¼ĀĒ·ūŗÅ£©£¬¹ŹÉś³É1molĪų»ÆĒā£ØH2Se£©·“Ó¦ČČÓ¦ÅÅŌŚµŚ¶žĪ»£¬Ó¦ĪŖ+29.7kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗb£»
£Ø2£©¢ŁÓɹ¤ŅÕĮ÷³ĢĶ¼æÉÖŖ£¬µē½ā²ŪÖŠµē½āHBr£¬Éś³ÉH2ÓėBr2£¬·“Ó¦·½³ĢŹ½ĪŖ2HBr=H2+Br2£¬ÓɱķÖŠŹż¾ŻæÉÖŖ£¬”÷H=362kJ/mol”Į2-436kJ/mol-194kJ/mol=+94kJ/mol£¬¹ŹČČ»Æѧ·½³ĢŹ½ĪŖ2HBr£Øaq£©=H2£Øg£©+Br2£Øg£©”÷H=+94kJ/mol£¬
¹Ź“š°øĪŖ£ŗ2HBr£Øaq£©=H2£Øg£©+Br2£Øg£©”÷H=+94kJ/mol£»
¢Ś·ÖĄėŗóµÄH2SO4ČÜŅŗÓŚŹŌ¹Ü£¬ĻņĘäÖŠÖšµĪ¼ÓČėAgNO3ČÜŅŗÖĮ³ä·Ö·“Ó¦£¬Čō¹Ū²ģµ½ĪŽµ»ĘÉ«³Įµķ²śÉś£¬×īÖÕÉś³É°×É«³Įµķ£¬ĖµĆ÷·ÖĄėŠ§¹ū½ĻŗĆ£¬
¹Ź“š°øĪŖ£ŗĪŽµ»ĘÉ«³Įµķ²śÉś£¬×īÖÕÉś³É°×É«³Įµķ£»
¢ŪŌŚŌµē³ŲÖŠ£¬øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬SO2ŌŚøŗ¼«·ÅµēÉś³ÉH2SO4£¬µē¼«·“Ó¦Ź½ĪŖSO2+2H2O-2e-=4H++SO42-£¬¹Ź“š°øĪŖ£ŗSO2+2H2O-2e-=4H++SO42-£»
¢ÜŌŚµē½ā¹ż³ĢÖŠ£¬µē½ā²ŪŅõ¼«·¢Éś»¹Ō·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ2H++2e-=H2”ü£¬ĒāĄė×ÓÅØ¶Č½µµĶ£¬ČÜŅŗpH±ä“󣬹Ź“š°øĪŖ£ŗ±ä“ó£»
¢ŻŌµē³ŲÖŠµē³Ų×Ü·“Ó¦ĪŖSO2+Br2+2H2O=H2SO4+2HBr£¬µē½ā³ŲÖŠ×Ü·“Ó¦ĪŖ2HBr=H2+Br2£¬¹ŹøĆ¹¤ŅÕĮ÷³ĢÓĆ×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗSO2+2H2O=H2SO4+H2£¬øĆÉś²ś¹¤ŅÕµÄÓŵć£ŗäåæÉŅŌŃ»·ĄūÓĆ£¬»ńµĆĒå½ąÄÜŌ“ĒāĘų£¬
¹Ź“š°øĪŖ£ŗSO2+2H2O=H2+H2SO4£»Br2±»Ń»·ĄūÓĆ»ņÄÜŌ“Ń»·¹©øų»ņ»ńµĆĒå½ąÄÜŌ“£»
£Ø3£©ŗ£Ė®Ģįäå¹ż³ĢÖŠ£¬ĻņÅØĖõµÄŗ£Ė®ÖŠĶØČėĀČĘų£¬½«ĘäÖŠµÄBr-Ńõ»Æ£¬ŌŁÓĆæÕĘų“µ³öäå£»Č»ŗóÓĆĢ¼ĖįÄĘČÜŅŗĪüŹÕä壬äåŌŚĢ¼ĖįÄĘČÜŅŗµÄĘē»ÆæÉ°Ń·“Ó¦Ąķ½āĪŖäåÓėĖ®·¢ÉśĘē»Æ£¬²śÉśH+µÄ±»Ģ¼ĖįÄĘĪüŹÕ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ3£ŗBr2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-£Ø»ņ3 Br2+3CO32-=5 Br-+BrO3-+3CO2”ü£©£¬
¹Ź“š°øĪŖ£ŗCl2£»3 Br2+6 CO32-+3H2O=5 Br-+BrO3-+6HCO3-£Ø»ņ3 Br2+3CO32-=5 Br-+BrO3-+3CO2”ü£©£®
µćĘĄ ±¾Ģā×ŪŗĻŠŌ½ĻĒ棬Éę¼°ŌŖĖŲĶʶĻ”¢»Æѧ¹¤ŅÕĮ÷³Ģ”¢·“Ó¦ČČ”¢Ōµē³Ų¼°µē½āŌĄķ”¢ŗ£Ė®ĢįČ”ä唢»ÆŃ§Ę½ŗāŅĘ¶ÆµČ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ÄŃ¶Č½Ļ“ó£¬×¢Ņā»ł“”ÖŖŹ¶µÄČ«ĆęÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆÕō·¢µÄ·½·ØŹ¹NaCl“ÓČÜŅŗÖŠĪö³öŹ±£¬Ó¦½«Õō·¢ĆóÖŠNaClČÜŅŗŠ”»š¼ÓČČÕōøÉ | |
| B£® | ÅäÖĘ100ml1.00mol/LµÄNaClČÜŅŗ£¬ŠčÓĆĶŠÅĢĢģĘ½×¼Č·³ĘĮæ5.9gĀČ»ÆÄĘ¹ĢĢå | |
| C£® | ĄūÓĆÕōĮóµÄ·½·Ø½ųŠŠŅŅ“¼ÓėĖ®µÄ·ÖĄėŹ±£¬ĪĀ¶Č¼ĘĖ®ŅųĒņÓ¦·ÅŌŚŅŗĆęŅŌĻĀĄ“×¼Č·²ā¶ØĪĀ¶Č | |
| D£® | ÓĆÅØĮņĖįÅäÖĘŅ»¶ØĪļÖŹµÄĮæµÄÅØ¶ČµÄĻ”ĮņĖįŹ±£¬ĻņÅØĮņĖįÖŠ¼ÓĖ®Ļ”ŹĶ£¬ĄäČ“ÖĮŹŅĪĀŗó²ÅÄܹ»Ņʵ½ČŻĮæĘæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 2005Äź2ŌĀ£¬ĪŅ¹śÕžø®¾Ķŗ¬ÓŠĢķ¼Ó”°ĖÕµ¤ŗģŅ»ŗÅ”°É«ĖŲµÄŹ³Ę·æÉÄÜÓÕ·¢°©Ö¢·¢³ö¾Æøę£¬²¢Č«ĆęĒå½ĖĖÕµ¤ŗģ£®”°ĖÕµ¤ŗģŅ»ŗÅ”°½į¹¹¼ņŹ½ČēĶ¼£®ÓŠ¹Ų”°ĖÕµ¤ŗģŅ»ŗÅ”°µÄĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ £Ø””””£©
2005Äź2ŌĀ£¬ĪŅ¹śÕžø®¾Ķŗ¬ÓŠĢķ¼Ó”°ĖÕµ¤ŗģŅ»ŗÅ”°É«ĖŲµÄŹ³Ę·æÉÄÜÓÕ·¢°©Ö¢·¢³ö¾Æøę£¬²¢Č«ĆęĒå½ĖĖÕµ¤ŗģ£®”°ĖÕµ¤ŗģŅ»ŗÅ”°½į¹¹¼ņŹ½ČēĶ¼£®ÓŠ¹Ų”°ĖÕµ¤ŗģŅ»ŗÅ”°µÄĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ £Ø””””£©| A£® | ·Ö×ÓŹ½ĪŖC16H12N2O | |
| B£® | ÄÜÓėÅØäåĖ®·¢ÉśČ”“ś·“Ó¦ | |
| C£® | ÄÜÓėĀČ»ÆĢśČÜŅŗ×÷ÓĆŹ¹ČÜŅŗ³Ź×ĻÉ« | |
| D£® | ŅņĖÕµ¤ŗģŅ»ŗÅÖŠŗ¬ÓŠ·ÓōĒ»ł£¬¹Źæɱ»æÕĘųŃõ»Æ²śÉśČ©»ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| t”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com