
 ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
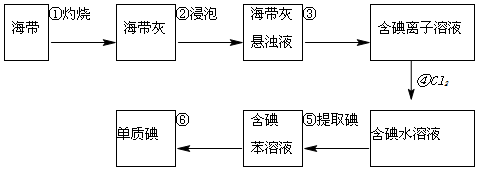
ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ·ÖĪö ŗ£“ų×ĘÉÕŗóµĆµ½ŗ£“ų»Ņ½žÅŻŗóµĆµ½ŗ£“ų»ŅµÄ×ĒŅŗ£¬¹żĀĖµĆµ½ŗ¬µāĄė×ÓµÄČÜŅŗĶØČėĀČĘųŃõ»ÆµāĄė×ÓĪŖµāµ„ÖŹ£¬µĆµ½ŗ¬µāĖ®ČÜŅŗ£¬¼ÓČėÓŠ»śČܼĮ±½£¬ŻĶČ”·ÖŅŗµĆµ½ŗ¬µāµÄ±½ČÜŅŗ£¬ĶعżÕōĮóµĆµ½µāµ„ÖŹ£¬
£Ø1£©×ĘÉÕŗ£“ųŹ±ŠčŅŖµÄŅĒĘ÷ŹĒŪįŪö£»
£Ø2£©¹żĀĖÄÜÓĆÓŚÄŃČÜŠŌ¹ĢĢåŗĶŅŗĢåµÄ·ÖĄė£¬¾Ż“ĖŃ”Ōń²£Į§ŅĒĘ÷£»
£Ø3£©·ÖĄėĮ½ÖÖ»„ČܵÄŅŗĢåÓĆÕōĮó½ųŠŠ£»
£Ø4£©ĀČĘų¾ßÓŠŃõ»ÆŠŌÄÜŃõ»ÆµāĄė×ÓÉś³Éµāµ„ÖŹ£»
£Ø5£©øł¾ŻŻĶČ”µÄ»ł±¾ŌŌņĮ½ÖÖČܼĮ»„²»ĻąČÜ£¬ĒŅČÜÖŹŌŚŅ»ÖÖČܼĮÖŠµÄČܽā¶Č±ČŌŚĮķŅ»ÖÖ“óµÄ¶ą½ųŠŠ½ā“š£»
£Ø6£©øł¾Żµāµ„ÖŹµÄĢŲŠŌĄ“¼ģŃ飮
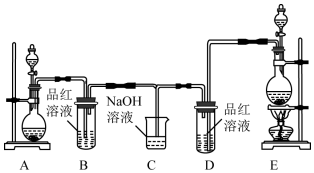
½ā“š ½ā£ŗ£Ø1£©×ĘÉÕ¹ĢĢåĪļÖŹŅ»°ćŹ¹ÓĆ£Ø“É£©ŪįŪö£¬¶ųŪįŪö¼ÓČČŠčŅŖÓĆĹȿ½ÅÖ§³ÅČ»ŗó·ÅŌŚČż½Å¼ÜÉĻ£¬Čż½Å¼ÜĻĀĆęµÄæÕ¼ä·Å¾Ę¾«µĘ£®¹Ź“š°øĪŖ£ŗBD£»
£Ø2£©²½Öč¢ŪŹĒ·ÖĄė¹ĢĢåŗĶŅŗĢ壬ŠčŅŖÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠÉÕ±”¢²£Į§°ō”¢Ā©¶·£¬
¹Ź“š°øĪŖ£ŗ¹żĀĖ£»ÉÕ±”¢²£Į§°ō”¢Ā©¶·£»
£Ø3£©ŹµŃé²Ł×÷ĪŖ¹żĀĖ£¬²½Öč¢ŽµÄÄæµÄŹĒ“Óŗ¬µā±½ČÜŅŗÖŠ·ÖĄė³öµ„ÖŹµāŗĶ»ŲŹÕ±½£¬ŹĒĄūÓĆ»„ČܵÄĮ½ÖÖŅŗĢåµÄ·Šµć²»Ķ¬Ą“·ÖĄė£¬ŌņŹµŃé²Ł×÷ĪŖÕōĮó£¬
¹Ź“š°øĪŖ£ŗÕōĮó£»
£Ø4£©²½Öč¢Ü·“Ó¦ŹĒµāĄė×Ó±»ĶØČėĀČĘųŃõ»ÆÉś³É£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2I-+Cl2=I2+2Cl-£¬
¹Ź“š°øĪŖ£ŗ2I-+Cl2=I2+2Cl-£»
£Ø5£©øł¾ŻŻĶČ”µÄ»ł±¾ŌŌņĮ½ÖÖČܼĮ»„²»ĻąČÜ£¬ĒŅČÜÖŹŌŚŅ»ÖÖČܼĮÖŠµÄČܽā¶Č±ČŌŚĮķŅ»ÖÖ“óµÄ¶ą£¬
¹Ź“š°øĪŖ£ŗ±½ÓėĖ®»„²»ĻąČÜ£¬µāŌŚ±½ÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠ“ó£»
£Ø6£©µāÓöµķ·Ū±äĄ¶É«£¬¼ģŃéĢįČ”µāŗóµÄĖ®ČÜŅŗÖŠŹĒ·ń»¹ŗ¬ÓŠµ„ÖŹµāµÄ¼ņµ„·½·Ø£ŗȔɣĮæĢįČ”µāŗóµÄĖ®ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė¼øµĪµķ·ŪŹŌŅŗ£»¹Ū²ģŹĒ·ń³öĻÖĄ¶É«£ØČē¹ū±äĄ¶£¬ĖµĆ÷»¹ÓŠµ„ÖŹµā£©£¬
¹Ź“š°øĪŖ£ŗȔɣĮæĢįČ”µāŗóµÄĖ®ČÜŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČė¼øµĪµķ·ŪŹŌŅŗ£¬¹Ū²ģŹĒ·ń³öĻÖĄ¶É«£¬Čē¹ū±äĄ¶£¬ĖµĆ÷»¹ÓŠµ„ÖŹµā£®
µćĘĄ ±¾Ģāæ¼²éŗ£Ė®×ŹŌ“µÄ×ŪŗĻĄūÓĆ£¬²ąÖŲæ¼²éĪļÖŹµÄ¼ģŃ锢»ģŗĻĪļµÄ·ÖĄėŗĶĢį“棬Ć÷Č·³£¼ū»ģŗĻĪļ·ÖĄėŗĶĢį“æ·½·Ø¼°ĘäєȔ·½·ØŹĒ½ā±¾Ģā¹Ų¼ü£¬³£¼ūµÄ·ÖĄė·½·ØÓŠ£ŗ¹żĀĖ”¢ÕōĮó”¢ÉųĪö”¢¼ÓČČµČ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬1 mol/L¼×ĖįČÜŅŗÖŠµÄc£ØH+£©Ō¼ĪŖ1”Į10-2mol•L-1 | |
| B£® | ¼×ĖįÄÜÓėĢ¼ĖįÄĘ·“Ó¦·Å³ö¶žŃõ»ÆĢ¼ | |
| C£® | 10 mL 1 mol•L-1¼×ĖįČÜŅŗĒ”ŗĆÓė10 mL 1 mol•L-1NaOHČÜŅŗĶźČ«·“Ó¦ | |
| D£® | ¼×ĖįČÜŅŗÓėŠæ·“Ó¦±ČĒæĖįČÜŅŗÓėŠæ·“Ó¦»ŗĀż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
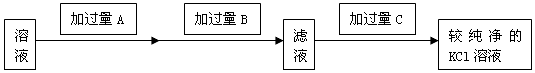
| A£® | Na2CO3ŗĶHCl | B£® | NaClŗĶNa2CO3 | C£® | H2SO4ŗĶBaCl2 | D£® | NaClŗĶNa2SO4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com