
下列混合溶液中,各离子浓度的大小顺序正确的是
A.10 mL0.1 mol·L-1NH4Cl溶液与5 mL0.2 mol·L-1NaOH溶液混合,
c(Na+)=c(Cl-)>c(OH-)>c(H+)
B.10 mL0.1 mol·L-1氨水与10 mL0.1 mol·L-1盐酸混合,
c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.10 mL0.1 mol·L-1CH3COOH溶液与10 mL0.2 mol·L-1NaOH溶液混合,
c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10 mL0.5 mol·L-1CH3COONa溶液与5 mL1 mol·L-1盐酸混合,
c(Cl-)>c(Na+)>c(OH-)>c(H+)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列反应中,属于氧化还原反应的是( )
A.2 H2O2  2 H2O + O2↑
2 H2O + O2↑
B.2 Al(OH)3  Al2O3 + 3 H2O
Al2O3 + 3 H2O
C.FeO + 2 HCl = FeCl2 + H2O
D. CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列反应的化学方程式:
①工业上电解饱和食盐水制取大量氯气
②实验室制氯气时用氢氧化钠溶液吸收尾气
③氯气和水反应
(2)配平下列化学方程式
① Cu+ HNO3→ Cu(NO3)2+ NO+ H2O
② KMnO4+ HCl→ MnCl2+ Cl2+ KCl+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在已经处于化学平衡的体系中,如果下列量发生变化,化学平衡一定发生了移动的是
A.反应混合物的浓度 B.反应体系的压强
C.正、逆反应的速率 D.反应体系的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子,能在指定溶液中大量共存的是
①无色溶液中:K+、Cl-、Na+、HCO3-、OH-
②使甲基橙变红的溶液中:MnO4-、NO3-、SO42-、Na+、Fe3+
③水电离的c(H+)=10-12mol·L-1的溶液中:ClO-、HCO3-、NO3-、NH4+
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、Na+、SO42-
⑤使pH试纸变深蓝色的溶液中: K+、CO32-、Na+、AlO2-
⑥pH=0的溶液中:Fe2+、Al3+、NO3-、Cl-、SO32-
A.①②③ B.②④⑤ C.①②⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 L HNO3和H2S04的混合溶液中,两种酸的物质的量浓度之和为O.6 mol/l,向该溶液中加入足量铜粉,加热,充分反应,当HNO3与H2S04的物质的量比为x:y 时所得溶液中Cu2+物质的量浓度最大,则x:y为
A.3:8 B.2:3 C.1:4 D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
吸食“摇头丸”会严重破坏中枢神经,其化学式为C9H13N,请回答:
2 mol“摇头丸”所含的碳原子的物质的量为______mol,氢原子的物质的量为______mol,氮原子的物质的量为______mol,氮原子的个数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)被称为21世纪界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)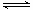 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g)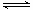 CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g)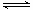 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为 。
A.加入某物质作催化剂 B.加入一定量CO C.反应温度降低 D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率
为 ;
若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a= mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g)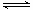 CH3OCH3(g)+CO2(g)的△H= 。
CH3OCH3(g)+CO2(g)的△H= 。
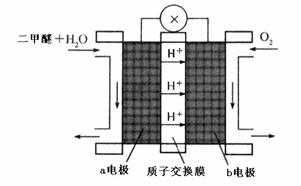
(4)“二甲醚燃料电池”是一种绿色电源,其工作原理如上图所示。b电极是 极,写出b电极上发生的电极反应式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com