
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
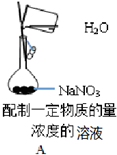
分析 A.容量瓶只能配制溶液,不能溶解或稀释药品;
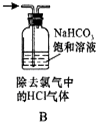
B.氯气、HCl都能和碳酸氢钠溶液反应;
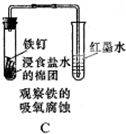
C.弱酸性或中性条件下,钢铁发生吸氧腐蚀;
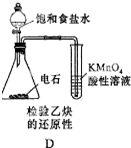
D.饱和食盐水和电石生成乙炔,生成的乙炔中还含有硫化氢等还原性气体,乙炔和硫化氢等还原性气体都能被酸性高锰酸钾溶液氧化.
解答 解:A.容量瓶只能配制溶液,不能溶解或稀释药品,应该先在烧杯中溶解硝酸钠,然后使溶液冷却至室温后,再转移到容量瓶中,故A错误;
B.氯气、HCl都能和碳酸氢钠溶液反应,应该用饱和食盐水除去氯气中的氯化氢,故B错误;
C.弱酸性或中性条件下,钢铁发生吸氧腐蚀,氯化钠溶液呈中性,铁钉发生吸氧腐蚀,导致左边试管中压强减小,导致导管中红墨水上升,所以能实现实验目的,故C正确;
D.饱和食盐水和电石生成乙炔,生成的乙炔中还含有硫化氢等还原性气体,乙炔和硫化氢等还原性气体都能被酸性高锰酸钾溶液氧化,硫化氢等还原性气体干扰乙炔的检验,所以用酸性高锰酸钾溶液检验乙炔制取必须除去杂质,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及金属腐蚀与防护、物质检验、除杂、溶液配制等知识点,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,易错选项是D.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 分子代号 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 16 | 18 | 26 |
| A. | 四种气体中至少有两种气体分子互为同分异构体 | |
| B. | 四种气体通入溴的四氯化碳溶液中,都能使其褪色 | |
| C. | 气体乙的分子内所有的原子在同一平面上 | |
| D. | 鉴别丙和丁两种气体,可以用高锰酸钾酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
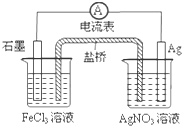
| A. | 导线上电子由Ag极流向石墨极 | B. | 负极电极反应式:Fe3++e-═Fe2+ | ||
| C. | 盐桥中阴离子移向AgNO3溶液 | D. | 总反应为:Fe3++Ag═Fe2++Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
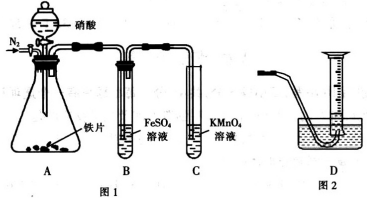 为探究铁和稀硝酸反应的产物,某兴趣小组进行如下实验.
为探究铁和稀硝酸反应的产物,某兴趣小组进行如下实验.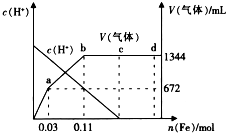
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)=c(HCO${\;}_{3}^{-}$) | |
| D. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe | ||
| C. | CaO+H2O═Ca(OH)2 | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com