
 ijС����ݹ�ҵ����ԭ���������ת����ϵ���Ի�ȡ�ռ�ͽ�����(Ti)��
ijС����ݹ�ҵ����ԭ���������ת����ϵ���Ի�ȡ�ռ�ͽ�����(Ti)��
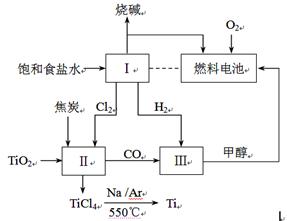
��1�� ȼ�ϵ����ͨ�������ĵ缫�� ������������������缫��Ӧʽ�� ���øõ�ص�ⱥ��ʳ��ˮ��������32 g�״��������Ϣ��п�����NaOH ________mol��
��2����ͼ��ʾ�������ϼ�����е�TiO2�ͽ�̿�����ʵ���֮���� ����TiCl4�õ�����Ti�Ļ�ѧ����ʽ�� ��
��3�����ݢ��кϳɼ״��ķ�Ӧ����С�鱣���¶Ȳ��䣬��������ͬ�ĺ����ܱ������н���ʵ�飬�й�ʵ���������£�
| ʵ���� | T/�� | ƽ��ʱѹǿ P/MPa | ��ʼ����/mol | ƽ��ʱCO��ת���� | �ų�����/kJ | |
| n(H2) | n(CO) | |||||
| �� | 250 | 2 | 20 | 10 | 90% | A |
| �� | 250 | P1 | 40 | 20 | c | B |
�� P1 4MPa�����������������������
��ʵ��������ºϳɼ״����Ȼ�ѧ����ʽ�� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±�Ϊ��ʽ���ڱ���һ���֣����еı�Ŵ�����Ӧ��Ԫ�ء�
| �� | ||||||||||||||||||
| �� | �� | |||||||||||||||||
| �� | �� | �� | �� | |||||||||||||||
| �� | �� | �� |
��ش��������⣺
(1)��������d��Ԫ�ص��� (��Ԫ�ط���)��
(2)����Ԫ�آٵ�6��ԭ����Ԫ�آ۵�6��ԭ���γɵ�ij�ֻ�״��������Ϊ ���ۺ͢��γɵ�һ�ֳ���
�ܼ��Ļ�ѧʽΪ �������幹��Ϊ________________��
(3)ijԪ��ԭ�ӵ���Χ�����Ų�ʽΪnsnnpn+1����Ԫ��ԭ�ӵ�������Ӳ��Ϲµ��Ӷ���Ϊ ����Ԫ����
Ԫ�آ����γɻ������ˮ��Һ�� �ԣ���ᡱ�����
(4)Ԫ�آܵĵ�һ������ Ԫ�آ�(ѡ���������������������)�ĵ�һ�����ܣ�Ԫ�آĵ縺�� Ԫ�آ�(ѡ���������������������)�ĵ縺�ԡ�
(5)Ԫ�آߺ͢��γɵĻ�����ĵ���ʽΪ ��
(6)Ԫ�آ�Ļ�̬ԭ�Ӻ�������Ų�ʽ�ǡ������� ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������������������ͿƼ��ȷ������������ȷ���ǣ� ��
A����������ͨ�ֺͲ�����е�̼������������
B�������Ƶ�ˮ��Һ�׳�ˮ������������ľ�ķ�����
C������ȼ�ŵ��̻���ijЩ����Ԫ�ط�����ɫ��Ӧ�����ֳ�����ɫ��
D����������Ȼˮ�����ɵ�Al(OH)3����������ˮ�������������ˮ�ľ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijѧ��Ϊ̽������CO2�ķ�Ӧ����������װ�ý���ʵ�顣����֪PdCl2�ܱ�CO��ԭ�õ���ɫ��Pd�����ɹ�ѡ���ҩƷ�У�CaCO3����״����Na2CO3����ĩ�������ᡢϡ���ᡢ�ơ�
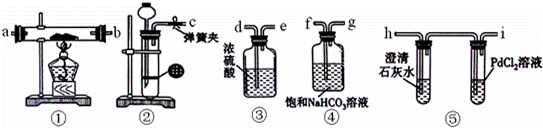
��1���뽫��ͼ��װ�������������ڡ� �� ���١� ������װ����ţ�
��2��װ�â��п����ϰ������ŵ�ҩƷ�ǣ� ��
��3�����װ�������Բ�װ��ҩƷ���۲쵽 ����ʱ�ŵ�ȼ�ƾ��ƣ��˲��������Ŀ���� ��
��4����֪CO�ڳ�ʪ�����пɽ�PdCl2��ԭΪ��ɫ��ĩ״���٣�Pd����д���÷�Ӧ�Ļ�ѧ����ʽ ��
��5��ʵ�������CO2������װ�â�PdCl2��Һ�й۲쵽�к�ɫ������װ�â��й���ɷ�ֻ��һ�֣���������м���ϡ���������ʹ����ʯ��ˮ����ǵ����塣�ݴ�����д��Na��CO2��Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и��������У�����˳����ȷ����
�� ��������ȶ��ԣ�Na2CO3��NaHCO3
�� ��ͬ���ʵ���Ũ�ȵ�������Һ��NH4+ ��Ũ�ȣ�
(NH4)2SO4��(NH4)2CO3��NH4Cl
�� ���뾶��K+��S2����F
�� �������ӵ�������CH3COOH��C2H5OH��H2O
�� �⻯��ķе㣺H2Se��H2S��H2O
A���٢� B���ڢ� C���٢� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪H��H����Ϊ436 KJ/mol��H��N����Ϊ391KJ/mol�����ݻ�ѧ����ʽ
N2 + 3H2 = 2NH3 ��H=��92.4 KJ/mol����N��N���ļ����� ( )
A��431 KJ/mol B��946 KJ/mol C��649 KJ/mol D��869 KJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
LiAl/FeS�����һ�����ڿ����ij��ص�أ��õ���������ĵ缫��ӦʽΪ��2Li����FeS��2e��===Li2S��Fe���йظõ�ص�����˵������ȷ����(����)��
A��LiAl�ڵ������Ϊ�������ϣ��ò�����Li�Ļ��ϼ�Ϊ��1��
B���õ�صĵ�ط�ӦʽΪ��2Li��FeS===Li2S��Fe
C�������ĵ缫��ӦʽΪ��Al��3e��===Al3��
D�����ʱ�����������ĵ缫��ӦʽΪ��Li2S��Fe��2e��===2Li����FeS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л�ѧ��Ӧ�У����������ֻ����� Ӧ���͵��ǣ� ����
Ӧ���͵��ǣ� ����
A��2FeCl3��Cu��2FeCl2��CuCl2 �� B��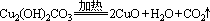
C��4Fe(OH)2+O2+2H2O= 4Fe(OH)3�� D��CaCO3��2HCl��CaCl2��H2O��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��Fe3O4��������ϡHNO3��Fe3O4��8H��=Fe2����2Fe3����4H2O
B�������ʵ�����MgCl2��Ba(OH)2 �� HC1 ��Һ��ϣ�Mg2����2OH��= Mg(OH)2��
C����������SO2ͨ��Ca(ClO)2��Һ�У� SO2+ClO��+H2O =HClO+ HSO3-
D����0.2 mol��L��1��NH4Al(SO4)2��Һ��0.3 mol��L��1��Ba(OH)2��Һ�������ϣ�
2Al3����3SO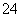 ��3Ba2����6OH��=2Al(OH)3����3BaSO4��
��3Ba2����6OH��=2Al(OH)3����3BaSO4��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com