
【题目】明矾[KAI(SO4)212H2O]是一种重要的化工产品,在生产、生活中都有广泛的用途。
某工厂计划利用炼铝厂的废料铝灰(含Al、A12O3、少量SiO2和FeOxFe2O3)为原料生产明矾产品,设计的生产工艺流程如下:
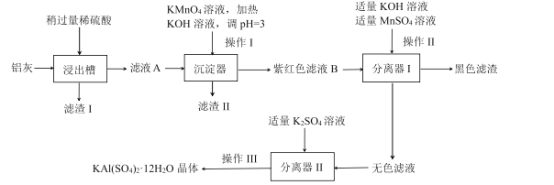
己知:![]()
请回答下列问题:
(1)检验滤液A中是否存在Fe2+,可用K3[Fe(CN)6]溶液,请写出其检验的离子反应方程式____。
(2)沉淀器中加入KMnO4溶液的作用是____;有人认为该生产流程较为复杂,可以用____溶液(填化学式)代替KMnO4溶液而使操作Ⅰ和操作Ⅱ过程得到优化。
(3)操作Ⅲ是 ___、____(填操作名称)、过滤、洗涤;在洗涤晶体时采用的洗涤剂最合适的是 ___(填正确答案标号)。
A.稀硫酸 B.蒸馏水 C.70%酒精
(4)明矾可作净水剂,其净水原理是 ____用离子方程式表示)。
(5)在沉淀器中调pH=3,请计算说明Fe3+是否完全沉淀(当Fe3+离子浓度小于或等于1.0x 10-5 mol/L时,可以认为溶液中无该离子)____。
【答案】2Fe(CN)63- +3Fe2+= Fe3[Fe(CN)6]2↓ 氧化Fe2+为Fe3+ H2O2 蒸发浓缩 冷却结晶 C Al3++3H2O![]() Al(OH)3(胶体)+3H+ 由
Al(OH)3(胶体)+3H+ 由![]() 可知,
可知,![]() ,所以Fe3+没有沉淀完全。
,所以Fe3+没有沉淀完全。
【解析】
铝灰含Al、A12O3、少量SiO2和FeOxFe2O3,加稀硫酸,得到滤渣∣为SiO2,滤液中含有Al3+、Fe2+、Fe3+,加入KMnO4溶液,氧化
Fe2+为Fe3+,加KOH溶液调节pH,将Fe3+反应生成Fe(OH)3的红褐色沉淀除去,所以滤渣Ⅱ为Fe(OH)3沉淀,紫红色溶液B中含MnO4-,加入MnSO4,发生歧化反应,生成MnO2的黑色固体,得到无色溶液中主要含有Al3+,加入K2SO4,生成明矾[KAI(SO4)212H2O]晶体。
(1)Fe2+与K3[Fe(CN)6]溶液反应生成Fe3[Fe(CN)6]2的蓝色沉淀,其离子反应方程式为:2Fe(CN)63- +3Fe2+= Fe3[Fe(CN)6]2↓,故答案为:2Fe(CN)63- +3Fe2+= Fe3[Fe(CN)6]2↓。
(2)KMnO4溶液具有强氧化性,氧化Fe2+为Fe3+,过氧化氢也具有强氧化性,也能将Fe2+氧化为Fe3+,可以用H2O2溶液代替KMnO4溶液,故答案为:氧化Fe2+为Fe3+;H2O2。
(3)得到明矾[KAI(SO4)212H2O]晶体,蒸发浓缩、冷却结晶、过滤、洗涤;[KAI(SO4)212H2O]易溶于水,也与稀硫酸反应,所以用70%的酒精洗涤晶体,故答案为:蒸发浓缩;冷却结晶;C。
明矾可作净水剂,[KAI(SO4)212H2O]中Al3+水解生成氢氧化铝的胶体,吸附水中悬浮的颗粒,其离子反应方程式为:Al3++3H2O![]()
Al(OH)3(胶体)+3H+,故答案为:Al3++3H2O![]() Al(OH)3(胶体)+3H+;
Al(OH)3(胶体)+3H+;
(5)pH=3,![]() ,由
,由![]() 可知,
可知,![]() ,所以Fe3+没有沉淀完全,故答案为:由
,所以Fe3+没有沉淀完全,故答案为:由![]() 可知,
可知,![]() ,所以Fe3+没有沉淀完全。
,所以Fe3+没有沉淀完全。


科目:高中化学 来源: 题型:
【题目】氧化铝陶瓷常用于厚膜集成电路,制备氧化铝陶瓷的合成路线如图所示,回答下列问题。
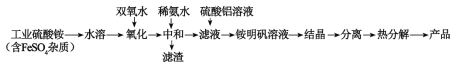
(1)“氧化”步骤发生的离子方程式为:___,使用双氧水作氧化剂优点为___:
(2)“热分解”得到的产物除了氧化铝外,还有NH3、N2、SO2、SO3、H2O生成,则氧化产物和还原产物的物质的量之比为___。
(3)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失重计算值”(失重计算值%=![]() ×100%)如表所示:
×100%)如表所示:
温度区间(℃) | 18→190 | 190→430 | 430→505 | 505→900 |
失重计算值(%) | 39.20 | 7.80 | 13.00 | 26.00 |
通过上述数据经粗略计算可判断,在温度区间___铵明矾基本上失去了全部结晶水。
(4)“结晶”步骤中常采用的操作是___。
(5)合成过程中常使用过量的工业硫酸铵,可利用硫酸铵溶液水解显酸性抑制硫酸铝水解,另外的一个重要作用是___。
(6)通常认为金属离子浓度等于1×10-5mol/L即可认为沉淀完全,试计算常温下“中和”步骤中需要调节溶液pH=___(保留一位小数,已知:Ksp[Fe(OH)3]=8.0×10-38,lg5=0.7)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】邻甲基苯甲酸主要用于农药、医药及有机化工原料的合成,其结构简式为 ,下列关于该物质的说法正确的是( )。
,下列关于该物质的说法正确的是( )。
A.该物质能与溴水生成白色沉淀
B.该物质含苯环的同分异构体中能水解且含有甲基的共5种
C.1mol该物质最多能与4molH2生加成反应
D.该物质中所有原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白铜是一种铜镍合金,为我国首先发明使用并传入世界各地,其发明在世界化学史和冶金史中都占有重要地位。白铜广泛用于造船、石油、化工、建筑、电力、精密仪表、医疗器械、乐器制作等部门作耐蚀的结构件。
(1)镍元素基态原子的电子排布式为______________,3d能级上的未成对电子数为______。
(2)单质铜、镍都是通过__________ 键形成晶体;比较元素铜与镍的第二电离能大小,I2(Cu)_____I2(Ni) (填“>”或“<”),原因是______________________。
(3)金属镍粉在CO气流中轻微加热,生成无色(或黄色)易挥发的液体Ni(CO)4。 写出一种与Ni(CO)4的配体互为等电子体的物质的分子式_____ ;推测Ni(CO)4的晶体类型是_______。呈正四面体构型的Ni( CO)4。易溶于下列物质中的______(填字母)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(4)N和Cu元素形成的化合物的晶胞结构如图所示,则该化合物的化学式为______该化合物的摩尔质量为M g●mol-1, NA代表阿伏加德罗常数的值。若该晶胞的边长为a pm,则该晶体的密度是_____g .cm-3。
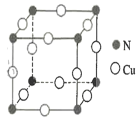
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列是中学化学中熟悉的物质:
O2 金刚石 NaBr H2SO4 Na2CO3 Na2S NaHSO4
回答下列问题:
这些物质中,只含共价键的是________;只含离子键的是________;既含离子键又含共价键的是________。
(2)写出下列物质的电子式。
Na2O2:_________________;
NH4H:_______________________;
(3)写出下列物质的结构式。
CO2:____________________
H2O2:_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,11.2 LHCl气体中含有的分子数为0.5NA
B. 常温常压下,5.6 g N2和CO混合物中所含有的原子数为0.4NA
C. 将0.2 mol FeCl3水解制成胶体,所得胶体粒子数为0.2NA
D. 50 mL12 mol/L盐酸与足量MnO2共热,转移电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸是一种强酸,氯酸的浓度超过40%就会迅速分解,反应的化学方程式为8HClO3=3O2↑+2Cl2↑+4HClO4+2H2O。根据题意完成下列小题:
①在上述变化过程中,发生还原反应的过程是_____→____(填化学式)。
②该反应的氧化产物是________(填化学式)。
(2)已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、MnO4-、IO4-。有关反应的离子方程式为_____。
(3)工业尾气中含有大量的氮氧化物,NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
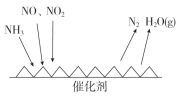
①由上图可知SCR技术中的氧化剂为_____________。
②用Fe作催化剂加热时,在氨气足量的情况下,当NO2与NO的物质的量之比为1∶1时,写出该反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途。完成下列填空:
(1) 实验室配制氯化铝溶液时加入盐酸的目的是____________。
(2)往AlCl3溶液中加入过量下列溶液,最终得到无色澄清溶液的是______(填编号)。
a Na2CO3 b NaOH c NaAlO2 d H2SO4
取AlCl3溶液,用小火持续加热至水刚好蒸干,生成白色固体的组成可表示为:Al2(OH)nCl(6-n),为确定n的值,取3.490g白色固体,全部溶解在0.1120 mol的HNO3(足量)中,并加水稀释成100 mL,将溶液分成两等价,进行如下实验:
(3)一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得Al2O3的质量为1.020g。判断加入氨水已足量的操作是________。过滤、洗涤后至少要灼烧_______次(填写数字);测定样品中铝元素含量时不选择测定干燥Al(OH)3的质量,而是测定A12O3的质量的原因可能是____(选填编号)。
a 干燥Al(OH)3固体时易失水 b Al2O3的质量比Al(OH)3大,误差小
c 沉淀Al(OH)3时不完全 d 灼烧氧化铝时不分解
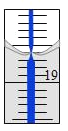
(4)从另一份溶液中取出20.00 mL,用0.1290 mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00 mL,终点时滴定管液面(局部)如图所示(背景为白底蓝线的滴定管)。则滴定管的读数__________mL,Al2(OH)nCl(6-n)中n的值为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法中正确的是( )
①该化合物仅含碳、氢两种元素 ②该化合物中碳、氢原子个数比为1∶4
③无法确定该化合物是否含有氧元素 ④该化合物中一定含有氧元素
A. ①②B. ②④C. ③④D. ②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com