
| A. | 碳酸钙与稀盐酸混合:CO32-+2H+=CO2↑+H2O | |
| B. | 硫酸铜溶液与烧碱溶液混合:Cu2++2OH-=Cu(OH)2↓ | |
| C. | 碳酸氢钠与稀盐酸混合:HCO3-+H+=CO2↑+H2O | |
| D. | 铁粉跟稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
分析 A.碳酸钙在离子反应中保留化学式;
B.反应生成硫酸钠和氢氧化铜;
C.反应生成氯化钠、水、二氧化碳;
D.反应生成氯化亚铁和氢气.
解答 解:A.碳酸钙与稀盐酸混合的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故A错误;
B.硫酸铜溶液与烧碱溶液混合的离子反应为Cu2++2OH-=Cu(OH)2↓,故B正确;
C.碳酸氢钠与稀盐酸混合的离子反应为HCO3-+H+=CO2↑+H2O,故C正确;
D.铁粉跟稀盐酸反应的离子反应为Fe+2H+=Fe2++H2↑,故D错误;
故选AD.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:选择题
| A. | x+y<n | B. | 该化学平衡向正方向移动 | ||
| C. | B的转化率增大 | D. | C的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量硫酸亚铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 | |
| B. | 硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量硫酸亚铁铵晶体放入试管,加入浓氢氧化钠溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下11.2L的水中含有0.5 NA个水分子 | |
| B. | 22.4LN2所含的电子数是14NA个 | |
| C. | 常温常压下,1 mol N2和NO的混合气体中含2NA个原子 | |
| D. | 含107g Fe(OH)3的胶体中胶粒总数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2与SO2完全反应时转移电子数为NA | |
| B. | 18g重水(D2O)所含的电子数为10NA | |
| C. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5 NA | |
| D. | 常温常压下,3gHCHO和CH3COOH的混合物中含有0.4NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
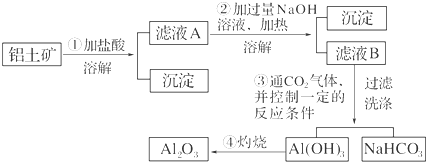
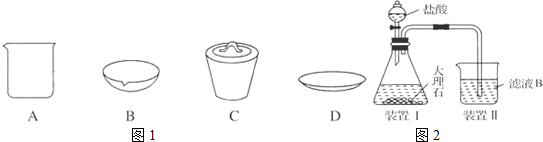
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ②③④⑤ | C. | ①③⑤⑥ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上第一次月考化学卷(解析版) 题型:选择题
图中的曲线表示的是其他条件一定时,反应:2NO+02 2N02 △H<0中N0的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)﹤v(逆)的点是 ( )
2N02 △H<0中N0的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)﹤v(逆)的点是 ( )
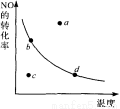
A.a点 B.b点 C. c点 D.d点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com