
【题目】物质的量浓度为c mol/L,体积为V mL的AgNO3溶液分别与100 mL NaCl、MgCl2、AlCl3溶液恰好完全反应,则这三种溶液的物质的量浓度之比为
A.6∶3∶2 B.1∶2∶3 C.2∶3∶6 D.2∶6∶3
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】用铝制易拉罐收集满CO2,加入过量NaOH浓溶液,立即把口封闭。发现易拉罐“咔咔”作响并变瘪了,过了一会儿,易拉罐又作响并鼓起来,下列有关判断正确的是
A.导致易拉罐变瘪的离子反应是CO2+OH![]()
![]()
B.导致易拉罐又鼓起来的反应是Al3++3![]()
![]() Al(OH)3↓+3CO2↑
Al(OH)3↓+3CO2↑
C.上述过程中共发生了三个化学反应,且反应结束后的溶液呈碱性
D.若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.0.2 mol NaOH含有0.2NA个NaOH分子
B.3.2 g O2和O3的混合气体中氧原子数为0.25NA
C.常温下,1 mol Cl2与过量NaOH溶液反应,转移电子总数为NA
D.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1 摩尔任何物质都含有 6. 02×1023 个分子
B. 摩尔是国际单位制中 7 个基本物理量之一
C. 含有 6.02×1023 个氧原子的H3PO4的物质的量是 0.25mol
D. 氧气的摩尔质量等于它的相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3在现代工业生产中应用广泛。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下探究实验,请回答下列问题:
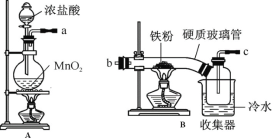
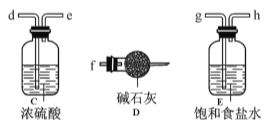
(1)装置的连接顺序为 (用a 、b、c…h表示)。
(2)i.A装置中反应的化学方程式为 。
ii.D中碱石灰的作用是 。
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。要使沉积得FeCl3进入收集器,需进行的操作是 。
(4)FeCl3溶液常用于吸收有毒气体H2S。反应的离子方程式为 。
(5)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(过程中不振荡),充分反应后,进行如下实验:

淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为 。
(6)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
根据上述实验得出溶液褪色的原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是( )
A.m、n
B.3、7
C.m﹣2、10﹣n
D.m+2、n+10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石墨为电极,电解足量KI溶液(并中含有少量酚酞和淀粉)。下列说法正确的是
A. 阳极附近溶液呈无色 B. 溶液的pH变大
C. 阳极逸出气体 D. 阴极附近溶液呈蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com