
下列过程表达式中,属于电离方程式的是
A.HCO3- + H2O 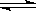 H2CO3 + OH- B.HCO3- + OH- ==== H2O + CO32-
H2CO3 + OH- B.HCO3- + OH- ==== H2O + CO32-
C.NH3 + H+ === NH4+ D.NH3·H2O 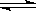 NH4+ + OH-
NH4+ + OH-
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同。根据甲、乙的摩尔质量(M)的关系判断,下列说法中正确的是( )
A.若M(甲)<M(乙),则分子数:甲<乙
B.若M(甲)>M(乙),则气体摩尔体积:甲<乙
C.若M(甲)<M(乙),则气体的压强:甲>乙
D.若M(甲)>M(乙),则气体的体积:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1 mol N2与足量的H2反应,转移的电子数是0.6NA
B.常温下,0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA
C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA
D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A化学反应必然伴随能量变化。
B、需加热才能发生的化学反应一定是吸热反应。
C、化学反应中的能量变化主要是由化学键的断裂和形成引起的。
D、反应物与生成物总能量的相对大小决定反应是吸热或放热。
查看答案和解析>>
科目:高中化学 来源: 题型:
右图曲线a表示放热反应X(g)+Y(g)  Z(g)+M(g)+N(s) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b
Z(g)+M(g)+N(s) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b
曲线进行,可采取的措施是
A、升高温度 B、加大X的投入量
C、加催化剂 D、增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
向0.l mol/L CH3COOH溶液中加入少量CH3COONa晶体时,会引起
A.溶液的pH增大 B.CH3COOH电离程度增大
C.溶液的导电能力减弱 D.溶液中c(OH-) 减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于酚的说法不正确的是( )
A.酚类是指羟基直接连在苯环上的化合物
B.酚类都具有弱酸性,在一定条件下可以和NaOH溶液反应
C.酚类都可以和浓溴水反应生成白色沉淀,利用该反应可以检验酚
D.分子中含有羟基和苯环的含氧衍生物都属于酚类
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g)2Z(g) ΔH<0。一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A.反应前2 min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前v逆>v正
C.保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,n(Z)<0.24 mol
D.其他条件不变,向平衡体系中再充入0.16 mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com