
| A. | ④ | B. | ③⑥ | C. | ①② | D. | ③⑤ |
分析 ①MnO4-为紫色;
②pH=1的溶液显酸性;
③加入Al能放出H2的溶液,为非氧化性酸或强碱溶液;
④由水电离的c(OH-)=10-13mol/L的溶液,为酸或碱溶液;
⑤Fe3+与SCN-结合生成络离子,Fe3+与HCO3-相互促进水解;
⑥酸性溶液中离子之间发生氧化还原反应.
解答 解:①MnO4-为紫色,与无色不符,故不选;
②pH=1的溶液显酸性,不能大量存在CO32-、AlO2-,故不选;
③加入Al能放出H2的溶液,为非氧化性酸或强碱溶液,强碱溶液中不能大量存在HCO3-、NH4+,酸溶液中不能大量存在HCO3-,故不选;
④由水电离的c(OH-)=10-13mol/L的溶液,为酸或碱溶液,酸碱溶液中该组离子之间不反应,可大量共存,故选;
⑤Fe3+与SCN-结合生成络离子,Fe3+与HCO3-相互促进水解,不能共存,故不选;
⑥酸性溶液中H+、NO3-、I-发生氧化还原反应,不能共存,故不选;
故选A.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意水解、氧化还原反应的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 硝酸钠、氢氧化钠 | B. | 氧化铜、二氧化锰 | C. | 二氧化锰、氯化钾 | D. | 硫酸铜、氢氧化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 待提纯的物质 | 除杂的试剂 | 操作方法 |
| A | NO2(NO) | O2 | 收集气体 |
| B | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| C | FeCl2溶液(FeCl3) | 足量铁粉 | 过滤 |
| D | KCl溶液(MgCl2) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 | |
| B. | 将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体 | |
| C. | 失去标签的硝酸银溶液、稀盐酸、氢氧化钠溶液、氯化铝溶液,可以用碳酸铵溶液鉴别 | |
| D. | 检验从火星上带回来的红色物体是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
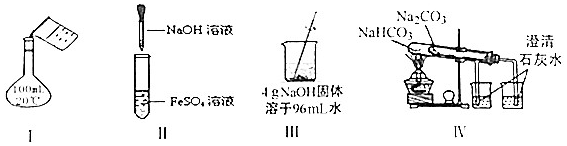
| A. | 实验Ⅰ:配制150mL0.10mol/L盐酸 | B. | 实验II:制取Fe(OH)2 | ||
| C. | 实验Ⅲ:配制4%NaOH溶液 | D. | 实验Ⅳ:比较两种物质的热稳定性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com