
向下列液体中滴加稀硫酸,开始时生成沉淀,继续滴加稀H2SO4沉淀又溶解的是
A.Na2CO3溶液 B.BaCl2溶液 C.NaAlO2溶液 D.Fe(OH)3胶体
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学试卷(解析版) 题型:选择题
下列化学用语正确的是
A.NaHCO3的水解:HCO3-+H2O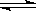 H3O++CO32-
H3O++CO32-
B.醋酸铵的电离:CH3COONH4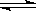 CH3COO-+NH4+
CH3COO-+NH4+
C.H2的燃烧热为285.8kJ/mol:H2(g)+ 1/2O2(g)=H2O(g);△H=-285.8kJ/mol
D.碳在高温下还原二氧化硅 SiO2+2C Si+2CO↑
Si+2CO↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二12月月考化学试卷(解析版) 题型:填空题
填空题,按要求回答下列问题:
(1)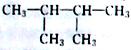 的系统命名为_________________;
的系统命名为_________________;
(2)3—甲基—2—戊烯的结构简式为_________________;
(3)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体。
①试写出它的一种链式结构的同分异体的结构简式_________________________。
②它有一种同分异体体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为_________________形。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川阆中中学校高二上第二次段考化学试卷(解析版) 题型:选择题
在2 L密闭容器中发生反应4A(s)+3B(g) == 2C(g)+D(g),经2 min,B的物质的量减少0.6 mol,下列对该反应速率表示正确的是
A.在2 min末的反应速率:v (B) = 0.3 mol·L-1·min-1
B.用A表示的反应速率为:v (A) = 0.4 mol·L-1·min-1
C.用D表示的平均反应速率为:v (D) = 0.05 mol·L-1·min-1
D.分别用B、C表示的反应速率其比值为2∶3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津静海一中高一上12月学业调研化学卷(解析版) 题型:填空题
(1)已知:2Fe3++2I-===2Fe2++I2, 2Fe2++Br2===2Fe3++2Br-。
①根据以上方程式比较Fe2+、Br-、I-还原性的强弱
②含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是________
(2)在硫酸铝、硫酸钾和明矾的1 L混合溶液中,如果SO42-浓度为0.4 mol/L,当加入等体积0.4 mol/L KOH溶液时,生成的沉淀恰好完全溶解,反应后混合溶液中K+的浓度为_______mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津静海一中高一上12月学业调研化学卷(解析版) 题型:选择题
钠在空气中发生变化的过程是
A.Na→Na2O2→NaOH→Na2CO3·10H2O→Na2CO3
B.Na→Na2O→NaOH→Na2CO3·10H2O→Na2CO3
C.Na→Na2O2→NaOH→Na2CO3→NaHCO3
D.Na→Na2O→NaOH→Na2CO3→NaHCO3
查看答案和解析>>
科目:高中化学 来源:2016届天津市高三上12月学业调研化学试卷(解析版) 题型:选择题
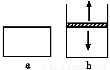
在一定温度下,a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等。在a、b中分别加入2 mol A和2 molB,起始时容器体积均为V L,发生反应2A+B 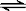 x C,并达到化学平衡状态,平衡时两容器中A、B、C的物质的量之比均为1:3:6。下列说法一定正确的是
x C,并达到化学平衡状态,平衡时两容器中A、B、C的物质的量之比均为1:3:6。下列说法一定正确的是
A.x的值为2
B.B物质可为固体或液体
C.平衡时,a容器的体积小于V L
D.a、b容器中从起始到平衡所需时间相同
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期12月阶段测化学试卷(解析版) 题型:实验题
现有以下实验装置供实验时挑选使用。
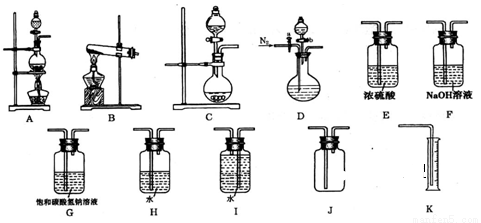
(1)利用Cu和浓硝酸反应制备NO2,用过氧化氢溶液和MnO2制取O2,根据反应原理应选用_______装置(填序号,从A、B、C中选取)。
(2)欲用石灰石和浓盐酸反应制取纯净干燥的CO2气体,将你所选的仪器按气体由左向右方向连接,连接顺序为: → G → → 。用饱和碳酸氢钠溶液除去挥发出的HCl优于用水除HCl的原因是_____________________。
(3)某小组为了探究Ag与浓硝酸反应过程中可能产生NO,设计了一连接顺序为D→H→I→K的实验装置。
①反应开始前通入N2的目的是______________________,
②反应结束,若H瓶中溶液体积为100mL,从中取出25.00mL溶液以酚酞作指示剂,用0.1000mol·L—1NaOH溶液进行滴定,两次滴定用去NaOH溶液的体积分别为16.98mL和17.02mL,则该瓶中硝酸的物质的量浓度为_______________。若实验测得NO的体积为95.2mL(已折算成标准状况),请你通过数据说明Ag与浓硝酸反应过程中________(填“是”或“否”)有NO产生。
(4)某同学设计下列四种制备NH3的方法,不合理的是_________(填序号)
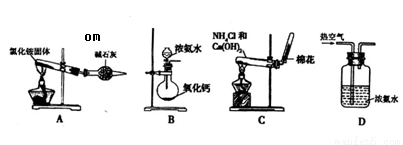
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附属中学高一上三次阶段测化学卷(解析版) 题型:填空题
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出 性质。
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于 (填“酸性”、“碱性”或“两性”,下同)氧化物,Al2O3属于 氧化物。
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是 ;
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com