

分析 Ⅱ.(1)仪器a的名称是 分液漏斗;E装置目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应;
(3)根据将Na2S2O3结晶析出的操作分析;
Ⅲ.【探究与反思】
(1)根据:Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl;硝酸、硫酸、盐酸等性质比较可知;
(2)根据亚硫酸钠易被氧化生成硫酸钠分析;
(3)根据重结晶的适用范围分析.
解答 解:Ⅱ.(1)仪器a的名称是分液漏斗;E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应,
故答案为:分液漏斗;B;
(3)将Na2S2O3结晶析出的操作应为:蒸发、结晶、过滤、洗涤、干燥,
故答案为:蒸发;
Ⅲ.【探究与反思】
(1)根据:Na2S2O3•5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl,以及硝酸具有强氧化性、加入硫酸会引入硫酸根离子可知,取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na2SO3和Na2SO4,
故答案为:过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸;
(2)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,防止Na2SO3被空气中的氧气氧化,
故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;防止Na2SO3被空气中的氧气氧化;
(3)Na2S2O3•5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯,
故答案为:重结晶.
点评 本题以某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O)为载体,考查了物质的分离提纯、检验、设计优化等,综合性较强.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线:
)具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线: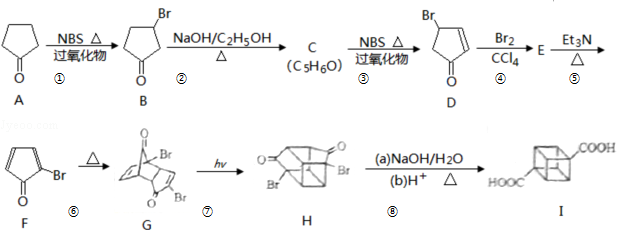
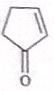 .
.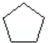 $\stackrel{反应1}{→}$X$\stackrel{反应2}{→}$Y$\stackrel{反应3}{→}$
$\stackrel{反应1}{→}$X$\stackrel{反应2}{→}$Y$\stackrel{反应3}{→}$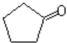 反应I的试剂与条件为Cl2/光照,反应2的化学方程式为
反应I的试剂与条件为Cl2/光照,反应2的化学方程式为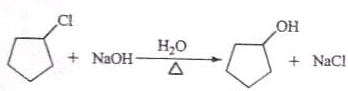 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.lmo/L的H2S溶液中:c(HS-)+c(S2-)=0.lmo/L | |
| B. | 常温下,100 mL pH=2的盐酸与10 mL pH=13的NaOH溶液混合,所得溶液pH=7 | |
| C. | 0.lmo/L CH3COOK溶液和0.lmo/L KOH溶液等体积混合,混合溶液中浓度大小关系是:c(K+)>c(CH3COO-)>c (OH-)>c(CH3COOH) | |
| D. | 0.lmo/L的三种溶液:①(NH4)2CO3 ②(NH4)2SO4 ③(NH4)2 Fe(SO4) 2 其c(NH4+)从大到小的顺序为:③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2FeO4是新型水处理剂,其原理与明矾相同 | |
| B. | Fe2O3俗称铁红,常用作红色油漆和涂料 | |
| C. | 推广应用燃料“脱硫、脱硝”技术,可减少硫氧化物和氮氧化物对空气的污染 | |
| D. | Al2O3熔点高,可用于制作耐高温仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| C. | H3O+和NH4+具有的电子数相同 | |
| D. | 用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用煤液化技术,可减少二氧化碳等温室气体的排放 | |
| B. | 加强化石燃料的开采利用,能从根本上解决能源危机 | |
| C. | 减少机动车尾气的排放,可以降低雾霾的发生 | |
| D. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙中C的转化率为75% | |
| B. | 反应达到平衡前,甲中始终有v正大于v逆,乙中始终有v正小于v逆 | |
| C. | 在该条件下,反应 2C(g)?A(g)+3B(g)的平衡常数为27×1.54(mol/L)2 | |
| D. | 乙中的热化学方程式为2C(g)?A(g)+3B(g);△H=+Q2kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com