
| A. | 35Cl和37Cl中子数不同,所以它们的原子结构示意图、电子式、核外电子排布式、轨道表达式都不相同 | |
| B. | 两个不同原子的1s、2s、2p、3s、3P各亚层中电子的能量相同 | |
| C. | 短周期主族元素原子最外层电子数一定等于其最高化合价 | |
| D. | CO2通入Na2SiO3溶液中可以得到硅酸 |
分析 A.35Cl和37Cl的核外电子数均为17;
B.两不同原子各亚层中电子的能量不相同;
C.氧元素、氟元素没有最高正化合价;
D.碳酸的酸性比硅酸强.
解答 解:A.35Cl和37Cl的核外电子数均为17,它们的原子结构示意图、电子式、核外电子排布式、轨道表达式都相同,故A错误;
B.不同原子的原子同、原子半径越等不同,两不同原子各亚层中电子的能量不相同,故B错误
C.氧元素、氟元素没有最高正化合价,除氧、氟外,短周期其它主族元素原子最外层电子数等于其最高化合价,故C错误;
D.碳酸的酸性比硅酸强,CO2通入Na2SiO3溶液中可以得到硅酸,故D正确,
故选:D.
点评 本题考查核外电子排布、元素周期律、元素化合物性质,比较基础,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素W的气态氢化物与M的单质可发生置换反应 | |
| B. | 离子半径的大小顺序为W>M>Z>X>Y | |
| C. | 元素Z、M的单质在一定条件下均能和强碱溶液反应 | |
| D. | 元素X与Y可以形成5种以上的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
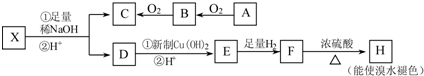
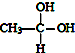 →CH3-CHO+H2O
→CH3-CHO+H2O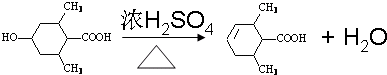 ;
;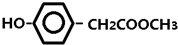 等.
等.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
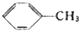 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$ $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$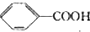
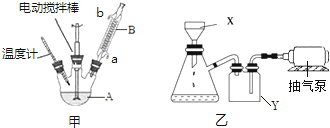
| 名称 | 相对分子质量 | 性状 | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 92 | 无色液体、易燃、易挥发 | -95 | 110.6 | 不溶 | 互溶 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 112.4(100℃升华) | 248 | 微溶 | 易溶 |
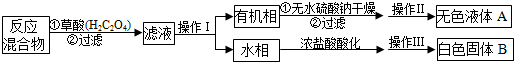
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向稀盐酸中加入少量钠粒:2Na+2H2O→2Na++2OH-?+H2↑ | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O→CaSO3↓+2HClO | |
| D. | 向含氯化铝的氯化镁溶液中加入氧化镁:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 砷元素的最高化合价为+3 | B. | 砷元素是第四周期的主族元素 | ||
| C. | 砷原子的次外层上有8个电子 | D. | 砷的氧化物的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
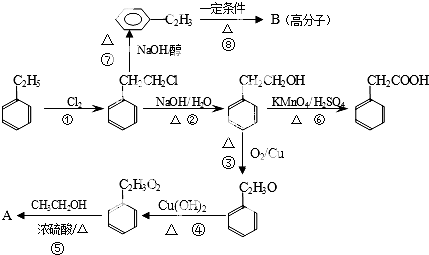
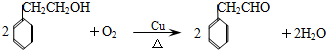
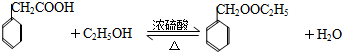
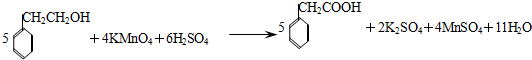

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与漂白粉溶液反应的离子方程式:Ca2++SO32-═CaSO3↓ | |
| B. | 通入SO2至过量:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] | |
| C. | 通入HCl至溶液pH=7:c(HSO3-)<c(Cl-) | |
| D. | 加入NaOH固体可使溶液中水的电离程度增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com