
已知25%氨水的密度为0.91g/cm3,5%氨水的密度为0.98g/cm3。若将上述两溶液等体积混合,所得氨水溶液的质量分数是( )
A.等于15% B.大于15%
C.小于15% D.无法估算
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
在常温下,将等体积的盐酸和氨水混和后,所得溶液的pH=7,则下列说法正确的是 ( )
A. 原来盐酸的物质的量浓度等于氨水的物质的量浓度
B. 所得溶液中c(NH4+)=c(Cl—)
C. 所得溶液中c(NH4+)+c(H+)=c(Cl—)
D. 所得溶液中c(NH4+)+c(NH3·H2O)=c(Cl—)
查看答案和解析>>
科目:高中化学 来源: 题型:
在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2IO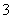 +5SO
+5SO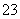 +2H+===I2+5SO
+2H+===I2+5SO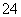 +H2O
+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示:
| 实验序号 | 0.01 mol·L-1 KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1 Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液出现蓝色时所需时间 |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
该实验的目的是________;表中V2=________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若某药品质量约为32 g,用托盘天平准确称其质量,若用↓表示在右 盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下。
盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下。
| 50 g | 20 g | 20 g | 10 g | 5 g |
(2) 配制500 mL 0.1 mol/L Na2CO3溶液,所需Na2CO3的质量为 g,实验时图中所示操作的先后顺序为 (填编号)。
配制500 mL 0.1 mol/L Na2CO3溶液,所需Na2CO3的质量为 g,实验时图中所示操作的先后顺序为 (填编号)。
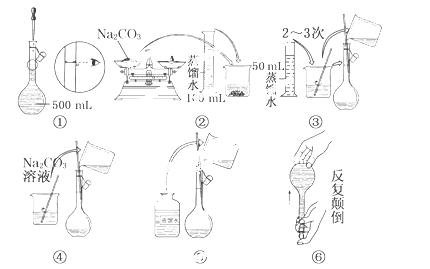
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响。
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度 。
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度 。
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用18 mol/L的硫酸配制100 mL 1.0 mol/L的硫酸,若实验仪器有:A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶 E.25 mL酸式滴定管 F.胶头滴管 G.50 mL烧杯 H.100 mL容量瓶
实验时所需仪器的先后顺序是(填入编号)____________________________________。
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1 cm~2 cm处,用滴管滴加蒸馏水到标线
D.配制溶液时,如果试样是液体,用滴定管量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1 cm~2 cm处,用滴管滴加蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转或摇动多次
查看答案和解析>>
科目:高中化学 来源: 题型:
利用实验器材(规格和数量不限)能够完成相应实验的一项是
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 三脚架、泥三角、坩埚、坩埚钳 | 煅烧石灰石制取生石灰 |
| B | 烧杯、玻璃棒、胶头滴管、100 mL容量瓶 | 用浓盐酸配制100mL 0.1 mol·L-1的稀盐酸溶液 |
| C | 烧杯、玻璃棒、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱工业是最基本的化学工业之一,其主要原理基于电解饱和食盐水:2NaCl+2H2O 2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
2NaOH+H2↑+Cl2↑,它的产品烧碱和氯气以及氢气应用广泛。请回答下列问题:
(1)电解前,如果粗盐中SO42- 含量较高,必须添加钡试剂除去SO42- ,该钡试剂可以是______________(填字母代号)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(2)“盐泥”是电解食盐水过程中形成的工业“废料”。某工厂的盐泥组成如下:
| 成分 | NaCl | Mg(OH)2 | CaCO3 | BaSO4 | 其他不溶物 |
| 质量分数(%) | 15~20 | 15~20 | 5~10 | 30~40 | 10~15 |
利用盐泥生产MgSO4·7H2O晶体的工艺流程如下图所示。
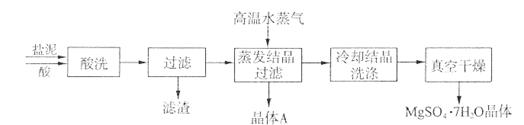
回答下列问题:
①酸洗过程中加入适量硫酸控制pH为5左右,反应温度在50℃左右。持续搅拌使之充分反应,以使Mg(OH)2充分溶解并转化为MgSO4,CaCO3在此过程中转化为CaSO4,请解释此转化得以发生的原因 。
②过滤所得滤渣的主要成分为 。
③根据下图分析,蒸发结晶过滤所得晶体A主要成分为 。
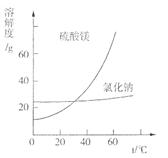
④真空干燥MgSO4·7H2O晶体的原因是 。
(3)已知NaCl在60 ℃的溶解度为37.1 g,现电解60 ℃精制饱和食盐水1371 g,经分析,电解后溶液密度为1.37 g·cm-3,其中含有20 g NaCl,则电解后NaOH的物质的量浓度为________________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
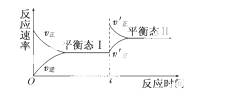 下图是恒温下化学反应“A(g)+B(g)
下图是恒温下化学反应“A(g)+B(g)  C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是 ( )
C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是 ( )
A.平衡态Ⅰ与平衡态Ⅱ的正反应速率相等
B.平衡移动的原因可能是增大了反应物浓度
C.平衡移动的原因可能是增大了压强
D.平衡状态Ⅰ和平衡状态Ⅱ的平衡常数的大小关系为K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
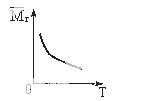
可逆反应2A+B 2C(g)+Q(Q>0)随T(℃)变化气体平均相对分子质量
2C(g)+Q(Q>0)随T(℃)变化气体平均相对分子质量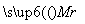 的变化如图所示,则下列叙述中正确的是( )
的变化如图所示,则下列叙述中正确的是( )
A.A和B可能都是固体 B.A和B一定都是气体
C.A和B可能都是气体 D.若B为固体,则A一定为气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com