(2013?淄博一模)氢溴酸在医药和石化工业上有广泛用途.如图是模拟工业制备氢溴酸的流程如图1:
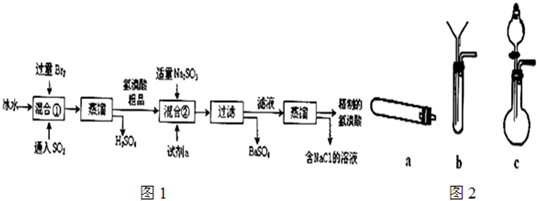
回答下列问题:
(1)混合①中发生反应的离子方程式为
SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
.
(2)混合②中加入试剂a是
BaCl2溶液
BaCl2溶液
.
(3)加入Na
2SO
3的目的是除去过量的Br
2,但要防止过量,原因是
SO32-+2H+=SO2↑+H2O
SO32-+2H+=SO2↑+H2O
(请用离子方程式表示).
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含Fe
3+②含Br
2③含Fe
3+和Br
2,只用下列一种试剂就能分析产生淡黄色的原因.该试剂是
e
e
(填写字母).
a.KMnO
4溶液 b.NaOH溶液 c.KSCN溶液 d.淀粉KI溶液 e.CCl
4(5)实验室制取Br
2的反应为:2NaBr+3H
2SO
4+NmO
22NaHSO
4+MnSO
4+Br
2↑+2H
2O 制取Br
2最好选用下列装置中的
c
c
(填写字母,固定和加热装置均已省略).简述检验图2装置气密性的方法
关闭分液漏斗活塞,将烧瓶上的导气管连接一段橡皮管并伸入水中,用手捂热烧瓶,若导管末端有气泡产生,冷却后导管中上升一段水柱,证明装置气密性良好
关闭分液漏斗活塞,将烧瓶上的导气管连接一段橡皮管并伸入水中,用手捂热烧瓶,若导管末端有气泡产生,冷却后导管中上升一段水柱,证明装置气密性良好
.




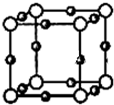 (2013?淄博一模)铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(2013?淄博一模)铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
 -OOCCH3
-OOCCH3 -OOCCH3
-OOCCH3




