
 CO2(g)+H2(g) 得到表中三组数据
CO2(g)+H2(g) 得到表中三组数据| 实验 | 温度℃ | 起始量/mol | 平均量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
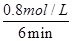 =0.13mol/(L?min)。又因为反应速率之比等于化学计量数之比,故v(CO2)=v(H2)=0.13mol/(L?min)。
=0.13mol/(L?min)。又因为反应速率之比等于化学计量数之比,故v(CO2)=v(H2)=0.13mol/(L?min)。 CO2(g)+H2(g)
CO2(g)+H2(g)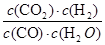 =
=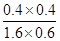 =0.17。
=0.17。

 考前必练系列答案
考前必练系列答案科目:高中化学 来源:不详 题型:单选题
| A.M+ | B.M2+ | C.M3+ | D.MO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 <_______。
<_______。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2mol | B.2.5mol | C.3mol | D.4mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.R3O4,RO,2 :1 | B.RO2,RO, 1:3 |
| C.RO2,R3O4 ,1 : 2 | D.RO2,RO,1 : 4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3:2 | B.3:5 | C.3:8 | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2CO(g) ΔH2="+172.5" kJ/mol ②
2CO(g) ΔH2="+172.5" kJ/mol ② 2CO(g)的平衡常数K=1.64,相同条件下测得高炉内c(CO)=0.2mol/L、c(CO2)=0.05mol/L,此时反应向_______(填“正”或“逆”)方向进行。
2CO(g)的平衡常数K=1.64,相同条件下测得高炉内c(CO)=0.2mol/L、c(CO2)=0.05mol/L,此时反应向_______(填“正”或“逆”)方向进行。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com