
| A. | 碳酸氢钠溶液与少量石灰水反应:HCO32-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| C. | 醋酸钠溶液和盐酸混合:CH3COONa+H+═CH3COOH+Na+ | |
| D. | 铁跟氯化铁溶液反应:Fe+2Fe3+═3Fe2+ |
分析 A.氢氧化钙少量,反应生成碳酸钠、碳酸钙和水;
B.氢氧化铁胶体不是沉淀,不能用沉淀符号;
C.醋酸钠为可溶性强电解质,应拆成离子形式;
D.二者反应生成氯化亚铁.
解答 解:A.碳酸氢钠溶液与少量石灰水反应,离子方程式:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故A错误;
B.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体,离子方程式:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故B错误;
C.醋酸钠溶液和盐酸混合,离子方程式:CH3COO++H+═CH3COOH,故C错误;
D.铁跟氯化铁溶液反应,离子方程式:Fe+2Fe3+═3Fe2+,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应知识是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷守恒规律,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 它们的原子序数B>A>C | B. | 它们的离子半径A2->C->B2+ | ||
| C. | 它们的原子半径C>B>A | D. | 它们的最外层电子数C>A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
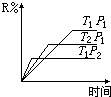 在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2S(?),此反应符合下面图象,下列叙述是正确的是( )
在密闭容器中进行下列反应:M(气)+N(气)?R(气)+2S(?),此反应符合下面图象,下列叙述是正确的是( )| A. | 正反应吸热,S是气体 | B. | 正反应吸热,S是固体 | ||
| C. | 正反应放热,S是气体 | D. | 正反应放热,S是固体或液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaHS溶液中滴入少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大 | |
| B. | 100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 | |
| C. | 0.1 mol•L-1 Na2SO3溶液加入少量NaOH固体,c(SO32-)与c(Na+)均增大 | |
| D. | 常温下pH=7的NaHSO3与Na2SO3混合溶液中:c(Na+)=c(HSO3-)+c(SO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | 四种短周期元素中W的原子半径最小 | |
| B. | Z元素在周期表中的位置是第三周期第ⅣA族 | |
| C. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| D. | 元素非金属性由强到弱的顺序:W>Z,W的单质常温下可与氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5.6的CH3COOH与CH3COONa混合溶液:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | 常温下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | NaHCO3溶液:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 浓度均为0.1mol/L的①NH4Cl ②NH3•H2O ③NH4HSO4 ④NH4HCO3四种溶液,c(NH4+)由大到小的顺序为:③>①>④>② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+ Na+ NO3- S2- | B. | Mg2+ H+ SO42- NO3- | ||
| C. | Al3+ Na+ HCO3- SO42- | D. | Fe3+ H+ SCN- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应都伴随有能量的变化 | |
| B. | 化学能与电能的相互转化必须通过一定的装置 | |
| C. | 太阳能、风能、氢能、电能都是可再生的新能源 | |
| D. | 能源的开发和利用情况可以衡量一个国家或地区的经济发展和科学技术水平 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com