


科目:高中化学 来源: 题型:阅读理解
| 编号 | 实验步骤 | 实验现象 | 化学方程式 | ||||||||
| ① | 将一小块钠放入滴有 酚酞溶液的冷水中 |
钠浮在水面上,熔成闪亮 的小球,四处游动,发出 嘶嘶的声音,最后消失, 溶液变为红色 |
2Na+2H2O=2NaOH+H2↑ | ||||||||
| ② | 将镁条用砂纸打磨 后,放入冷水中,滴 入几滴酚酞试液,然 后加热至沸腾; |
与冷水反应缓慢;加热煮沸有气体产生,溶液变为浅红色 | Mg+2H2O
Mg+2H2O
| ||||||||
| ③ | 将镁条投入稀盐酸中 | 强烈反应,迅速产生大量无色气体 | Mg+2HCl=MgCl2+H2↑ | ||||||||
| ④ | 将铝条投入稀盐酸中 | 比镁反应的速率慢一些,产生气体 | 2Al+6HCl=2AlCl3+3H2↑ 2Al+6HCl=2AlCl3+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
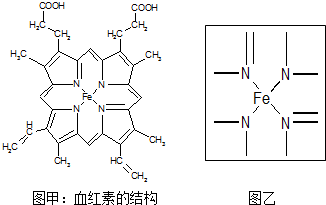


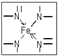

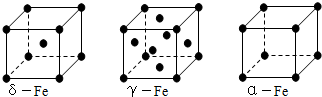
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.

| 3 |
| ||
| 3 |
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com