
下列各组离子在指定的溶液中能大量共存的是
A.强酸性溶液中:Na+、Fe2+、Cl-、ClO-
B.加入Al能放出的H2溶液中:Cl-、HCO3-、NO3-、NH4+
C.在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Fe2+、Al3+、NO3-、Cl-
D.pH=11的溶液中:CO32-、Na+、[Al(OH)4]-、NO3-
D
【解析】
试题分析: A.在强酸性溶液中含有大量的H+,H+、Fe2+、ClO-会发生离子反应,不能大量共存,错误; B.加入Al能放出的H2溶液可能显酸性,也可能显碱性,在酸性溶液中:H+、HCO3-会发生反应而不能大量共存;在碱性溶液中,OH-、HCO3-、NH4+会发生离子反应而不能大量共存,错误;C.在由水电离出的c(OH-)=10-13mol·L-1的溶液可能显酸性,也可能显碱性,在酸性溶液中:H+、Fe2+、NO3-会发生氧化还原反应而不能大量共存,在碱性溶液中Fe2+、Al3+会发生离子反应而不能大量共存,错误;D.pH=11的溶液是碱性溶液,在碱性溶液中,OH-、CO32-、Na+、[Al(OH)4]-、NO3-不能发生任何反应,可以大量共存,正确。
考点:考查溶液中离子大量共存的知识。


科目:高中化学 来源:2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷(解析版) 题型:填空题
(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题, 选学《有机化学基础》模块的考生.答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》:
(1)、(4分)良好的生态环境可以提升生活质量。
①提倡“光盘行动”,有利于“勤俭节约”、减少厨余垃圾,厨余垃圾的标识为 _ (填宇母)。

②下列物质中,不能用于饮用水杀菌消毒的是_ (填字母)。
a.漂白粉 b.乙醇 c.二氧化氯
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是_ (填字母)。
a.用中和法除去废水中的酸
b.用混凝剂除去废水中的重金厲离子
c.用氯气除去废水中的悬浮物
④某地区各空气污染物指数为S0278、NO2 43、可吸入颗粒物153。该地K的首要污染物为_ 。
(2)、(6分)保证食品安全,合理用药,是人体健康的基础。
①营养平衡、科学使用食品添加剂有助于健康和提髙免疫力。下列物质常用作食品防腐剂的是_ (填字母)。
a.苯甲酸钠 b.味精 c.柠橡黄
②下列药品属F国际奥委会严格禁止的兴奋剂是_ (填字母)。
a.阿司匹林 b.青霉素 c.吗啡
③氨基酸分子中含有的官能团是氨基(一NH2)和_ (写名称)。人体中共有 20多种氨基酸,其中人体自身_ (填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
④如何检验糖尿病患者的尿液中含有葡萄糖?写出实验操作方法、现象和结论:_
(3)、(5分)化学与材料密切关联。
①下列塑料可用作不粘锅的表血材料的是 (填字母)。
a.聚氯乙烯 b.聚四氟乙烯 c.有机玻璃
②下列关于铁制品保护措施的说法中不正确的有 (填字母)。
a.在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
b.将不锈钢制成刀其和餐具,有的刀具还进行烤蓝处理
c.在海轮的外壳上常焊有铜块,且定期更新
③钢筋泡凝土属于 材料。(填字母)
a.复合材料 b.无机非金属材料 c.金属材料
④氧气和四氯化硅蒸气在旋转的岛温炉中发生罝换反应,其产物之一可制得光导纤维,试写出该反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下述实验不能达到预期实验目的是
序号 | 实验内容 | 实验目的 |
A | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一会过滤 | 除去MgCl2中少量FeCl3 |
D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:填空题
(15分)氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:

(1)试剂X为_________(填化学式),发生反应的离子反应方程式为_________。
(2)滤渣2的成分是_________(填化学式)。
(3)操作3包括_________、冷却结晶、_________、洗涤、干燥等一系列操作,在此过程中玻璃棒的作用是_________(填代号)
①引流 ②搅拌加速溶解 ③搅拌使溶液受热均匀,防止暴沸
(4)煅烧过程存在以下反应:2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑ MgSO4+3C
MgO+SO2↑+CO↑ MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是_________(填化学式)。
②B中盛放的溶液可以是_________(填字母)。
A.NaOH溶液 b.Na2CO3溶液 c.KMnO4溶液 d.稀硝酸
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:_________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.工业上电解熔融的Al2O3冶炼铝用铁做阳极
B.用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子 转移,则生成2 molNaOH
转移,则生成2 molNaOH
D.用惰性电极电解CuSO4溶液一段时间后,加入CuO固体可以使CuSO4溶液恢复原来浓度
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关。下列有关说法中正确的是
A.顺丁橡胶、腈纶、涤纶和“人造棉花”都属于合成纤维
B.天官一号使用的碳纤维是一种新型有机高分子材料
C.绿色荧光蛋白质(GFP)是高分子化合物,不可降解,其水溶液 有丁达尔效应
有丁达尔效应
D.“玉兔”月球车太阳能电池帆板的材料是晶体硅
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三下学期期初联考化学试卷(解析版) 题型:选择题
一定条件下进行反应:A(g) B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(B)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法正确的是
A.反应前2min的平均速率v(B)=0.15 mol/(L·min)
B.保持其他条件不变,升高温度,平衡时c(B)=0.22 mol·L-1,则反应的ΔH < 0
C.保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小
D.保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,反应达到平衡前的速率:v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省五市十校高三下学期3月模拟考试理综化学试卷(解析版) 题型:实验题
【化学—选修2化学与技术】(15分)
氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:
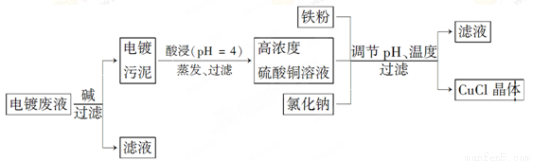
金属离子含量与混合液pH、CuCl产率与混合液pH的关系图如图。

【已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7】
请回答下列问题:
(1)酸浸时发生反应的离子方程式是________;析出CuCl晶体时的最佳pH在_______左右。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为________________。
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2 h、冷却密封包装。70℃真空干燥、密封包装的目的是_____________________________________。
(4)产品滤出时所得滤液的主要分成是________,若想从滤液中获取FeSO4·7H2O晶体,还需要知道的是__________________。
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式:____________________。为提高CuCl的产率,常在该反应体系中加入稀碱溶液,调节pH至3.5。这样做的目的是_____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省肇庆市高一上学期期末考试化学试卷(解析版) 题型:填空题
(8分)
(1)地壳中含量最高的金属是 ,NaHCO3俗称 ,制造计算机芯片的半导体材料是 ,水晶项链的主要成分是 。
(2)在反应 3Cu+8 HNO3(稀)== 3Cu(NO3)2+2NO↑+4H2O中,失去电子的是_____(填元素符号),被还原的是_____(填元素符号)。当产生标况下4.48 L气体时消耗单质铜_____g,此时转移了_____ mol电子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com