

分析 如CuO能氧化氨气,可生成NO或N2,实验时,A用于制备氨气,a为浓氨水,b为生石灰,B为反应装置,C用于检验是否生成水,如生成氮气,则通过F通入空气,D中无现象,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,实验时,A、B之间应加入干燥装置,以免为C的实验结果有影响,以此解答该题.
解答 解:如CuO能氧化氨气,可生成NO或N2,实验时,A用于制备氨气,a为浓氨水,b为生石灰,B为反应装置,C用于检验是否生成水,如生成氮气,则通过F通入空气,D中无现象,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,
(1)由以上分析可知a为浓氨水,b为生石灰,生石灰具有吸水作用,且放热,有利于氨气的挥发,故答案为:浓氨水;生石灰;
(2)A、B之间应加入干燥装置,以免为C的实验结果有影响,利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuS04变蓝,说明生成水,打开F导管上的止水夹,向广口瓶中鼓入空气,气体仍为无色,说明氨气被氧化生成氮气,则氨气与氧化铜反应的化学方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案为:A、B之间应加入干燥装置;2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)如上分析,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,故答案为:通入空气、尾气吸收装置.
点评 本题考查物质的性质实验的设计,为高考常见题型和高频考点,侧重于学生的分析、实验能力的考查,答题时注意物质的性质以及实验的原理和操作的严密性和合理性的评价,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
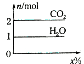 将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )| A | B | C | D | |
| 甲 | 戊烯 | 已烯 | 己二炔(C6H6) | 己烷 |
| 乙 | 环己烷(C6H12) | 苯 | 苯 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 立体烷 和苯乙烯 和苯乙烯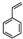 互为同分异构体 互为同分异构体 | |
| B. | 1,3-丁二烯的键线式可表示为 | |
| C. | 二氟化氧分子电子式为  | |
| D. | H216O、D216O、H218O、D218O互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 单质的氧化性:X>R>W | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | WX2和水反应形成的化合物是一定不能与铜反应 | |
| D. | 离子的氧化性:Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 920kJ | B. | 557kJ | C. | 436kJ | D. | 181kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气的燃烧热为△H=-285.5kJ•mol-1,则电解水的热化学方程式为2H2O(l)$\frac{\underline{\;电解\;}}{\;}$2H2(g)+O2(g)△H=+285.5k•Jmol-1 | |
| B. | 反应SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 | |
| C. | 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6k•Jmol-1 | |
| D. | 由C(石墨,s)=C(金刚石,s)△H=+1.90 k•Jmol-1可知,金刚石比石墨稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘酒是指碘单质的乙醇溶液 | |
| B. | 浓硫酸可以刻蚀石英制艺术品 | |
| C. | 84消毒液的有效成分是NaClO | |
| D. | 氢氧化铝、小苏打等可用于治疗胃酸过多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com