
| A�� | �����Ƿ绯���� | |
| B�� | �ڹ��ۢܢ�����Ԫ�ؾ������� | |
| C�� | ��ҵ�ϵ������״̬�µ��Ȼ�þ��ȡþ���� | |
| D�� | �����г�ȥ�����е�SO42-��Ca2+��Mg2+��Fe3+�����ʣ������ҩƷ˳��ΪNa2CO3��Һ��NaOH��Һ��BaCl2��Һ�����˺������ |
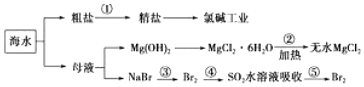
���� ��ˮͨ������Ũ���õ����κ�ĸҺ�����ξ��Ƴ�ȥ���ʵõ����Σ���ⱥ��ʳ��ˮ�õ��������ơ�������������ĸҺ�к���þ���Ӻ������ӣ�����ʯ�������þ���ӹ��˵õ�������þ��������Һ��������þ�ܽ��Ũ����������ȴ�ᾧ������ϴ�ӣ����Ȼ��������м���ʧȥ�ᾧˮ�õ���ˮ�Ȼ�þ����Һ�м�����������ˮ����������Ϊ�嵥�ʣ���ͨ������������պ��������������嵥�ʣ�
A���绯��ָijЩ���ᾧˮ�Ŀ�����ҩ������������Ӵ����վ�����ˮ����Ϊ��ĩ״̬��
B����Ԫ��ʧ���ӻ��ϼ�����ʱ��������
C����������Ȼ�þ���Ʊ�����þ��������
D����ȥ�����е�Ca2+��Mg2+��SO42-����ɳ�����Լӹ������Ȼ�����ȥ��������ӣ�Ȼ����̼����ȥ�������Ӻ����ı����ӣ�����Ҫ�����������ȥ�������������ƺ�̼���ƣ����������ƺ��Ȼ������Ⱥ�˳��Ҫ��
��� �⣺A���绯��ָijЩ���ᾧˮ�Ŀ�����ҩ������������Ӵ����վ�����ˮ����Ϊ��ĩ״̬���ù�����Ҫ���ȣ����Բ��Ƿ绯����A����
B���ڢ۲��У���Ԫ�ػ��ϼ۴�-1���ߵ�0�ۣ����������ڢܲ��У���Ԫ�ػ��ϼ۴�0���͵�-1�ۣ�����ԭ���ڢݲ��У���Ԫ�ػ��ϼ۴�-1���ߵ�0�ۣ�����������B����
C����ҵ�ϵ������״̬�µ��Ȼ�þ��������������ʧ���ӷ���������Ӧ����������������þ���ӵõ��������ɽ���þ����ȡþ���ʣ���C��ȷ��
D��ѡ���е��Լ�����˳���У��������������ȥ��������ҩƷ˳��Ϊ��BaCl2��Һ��NaOH��Һ��Na2CO3��Һ�����˺�����ᣬ��D����
��ѡC��
���� ���⿼���˺�ˮ��Դ���ۺ����ã��漰���ʵķ�����ᴿ������ѧ���������⡢���������������״�ѡ����D��ע����Ӽ������Ⱥ�˳��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2��CH4�����ȴ����ȶ����������ЧӦ����˶����ڴ�����Ⱦ�� | |
| B�� | �ⶨij���������귢�־���һ��ʱ��֮��pH�½����ж�Ϊ���������� | |
| C�� | ��̼������Ҫ�빤���������ŷ��йأ��������õ硢��ˮ����ֽ���Ƿ��Լ�� | |
| D�� | ��ɫ��ѧ�ĺ��������û�ѧԭ���Ի�����Ⱦ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7�� | B�� | 8�� | C�� | 9�� | D�� | 10�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѹǿ/MPa �������/% �¶�/�� | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A�� | 4�� | B�� | 3�� | C�� | 2�� | D�� | 1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ��̨�ϵ���ȼ���ױ�ҩƷҪԶ���Դ | |
| B�� | ���Ũ����մ��Ƥ����ӦѸ����Ĩ����ȥ�����ô���ˮ��ϴ�����Ϳ��С�մ���Һ | |
| C�� | ������Һ�ε�ʵ��̨�ϣ���ʪĨ�����ɾ�������ˮ��ϴ | |
| D�� | һ������ʵ��������ֻ��������Ӧ��������ѧУ�쵼��Ȼ����119���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ʵ��С����0.50mol/L KOH��Һ��0.50mol/L������Һ�����к��ȵIJⶨ��
ʵ��С����0.50mol/L KOH��Һ��0.50mol/L������Һ�����к��ȵIJⶨ��| ��Ŀ ���� ���� | ��ʼ�¶�T1/�� | ��ֹ�¶�T2/�� | �¶Ȳ�ƽ��ֵ ��T2-T1��/�� | ||
| H2SO4 | KOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 3 | 26.4 | 26.2 | 26.3 | 30.4 | |
| ʵ���� | ��Ӧ�� | ���� |
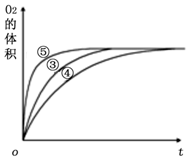
| �� | 10 mL 2% H2O2��Һ | �� |
| �� | 10 mL 5% H2O2��Һ | �� |
| �� | 10 mL 5% H2O2��Һ | 1 mL 0.1 mol•L-1 X��Һ |
| �� | 10 mL 5% H2O2��Һ+����HCl��Һ | 1 mL 0.1 mol•L-1 X��Һ |
| �� | 10 mL 5% H2O2��Һ+����NaOH��Һ | 1 mL 0.1 mol•L-1 X��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ���������O2��CH4�������Ϊ2��1 | |
| B�� | ��������ֻ��Na2CO3��NaOH | |
| C�� | ��Ӧ�е���ת������Ϊ0.8NA | |
| D�� | ����������Ϊ26.6�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
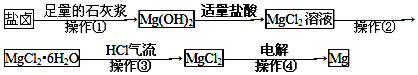
| A�� | ������--����Ϊ�˻����ˮ�Ȼ�þ | |
| B�� | �����ܷ�����������ԭ��Ӧ | |
| C�� | ����������ȴ�ᾧ | |
| D�� | ����ʵ���ҽ��в�����ֻ��Ҫ©�����ձ����ֲ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com