
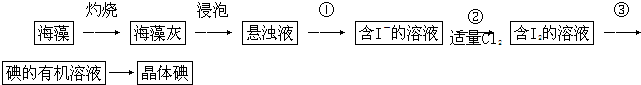


科目:高中化学 来源: 题型:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小 | ||
| B、C(s,石墨)=C(s,金刚石) 该反应吸热熵减,常压下,升温或者降温均为非自发反应 | ||
| C、在铁制品表面镀锌或者镀锡,都是采用外加保护层的方法来防止铁的腐蚀 | ||
D、向0.1mol/L CH3COOH溶液中加入少量的冰醋酸,溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
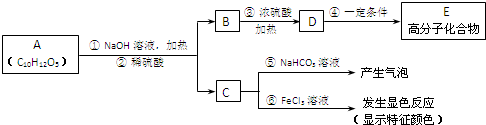
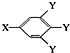 (其中:-X、-Y均为官能团).据此回答下列问题:
(其中:-X、-Y均为官能团).据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
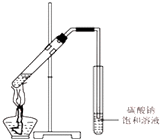 乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
| ② | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气态氢化物的稳定性:XH4>YH3>H2Z |
| B、元素非金属性强弱关系:X>Y>Z |
| C、最高价氧化物对应水化物酸性:H2XO3>H3YO4>H2ZO4 |
| D、原子半径:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用福尔马林对种子消毒不属于蛋白质变性 |
B、实验证实化合物 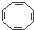 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 |
| C、能用新制的氢氧化铜鉴别乙醛与蔗糖溶液 |
D、化合物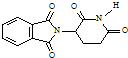 的分子式为C13H8O4N2 的分子式为C13H8O4N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
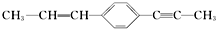 的描述正确的是( )
的描述正确的是( )| A、分子中的所有C原子一定在同一平面上 |
| B、分子中的所有原子可能在同一平面上 |
| C、除苯环外的其他C原子有可能在一条直线上 |
| D、除苯环外的其他C原子不可能在一条直线上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com