
【题目】X、Y、Z、W、R为五种短周期主族元素,Y、Z、W是原子序数递增的同周期相邻元素,且最外层电子数之和为15;X比Y核外少一个电子层;R的质子数是X、Y、Z、W四种元素质子数之和的![]() .下列说法正确的是( )
.下列说法正确的是( )
A. 简单离子半径:![]()
B. X与Y形成的二元化合物常温下一定为气态
C. W和R形成的化合物是离子化合物
D. Y与W、Z与W形成的二元化合物都是大气污染物
【答案】C
【解析】
X、Y、Z、M、W为五种短周期主族元素,Y、Z、W是原子序数依次递增的同周期元素,且最外层电子数之和为15,设Z的最外层电子数为m,则Y的最外层电子数为m-1,W的最外层电子数为m+1,即得出(m-1)+m+(m+1) = 3m = 15,所以m = 5,则推知Y、Z、W分别为C、N和O元素;X比Y核外少一个电子层,则X为H;又知R的质子数是X、Y、Z、W四种元素质子数之和的![]() ,则R的质子数为(6+7+8+1)×
,则R的质子数为(6+7+8+1)×![]() = 11,可知R为Na,然后结合元素周期律及元素化合物知识来解答。
= 11,可知R为Na,然后结合元素周期律及元素化合物知识来解答。
根据上述分析可知,X为H,Y为C,Z为N,W为O,R为Na,
A. 电子层数越大,简单离子半径越大,当电子层数相同时,其简单离子半径随原子序数的增大而减小,则N3- > O2- > Na+,即简单离子半径大小比较为:Z > W > R,故A项错误;
B. X与Y形成的二元化合物为烃类有机物,常温下可能为气态、液态或固态,故B项错误;
C. W和R形成的化合物为过氧化钠或氧化钠,成键微粒为阴阳离子,均为离子化合物,故C项正确;
D. Y与W形成的二元化合物为CO2或CO,其中CO为大气污染物,而CO2不是;Z与W形成的二元化合物为氮氧化物,为大气污染物,故D项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】将1 mol SO2和1 mol O2通入体积不变的密闭容器中,在一定条件下发生反应2SO2(g)+O2(g)![]() 2SO3(g),达到平衡时SO3为0.3 mol,此时若移走0.5 mol O2和0.5 mol SO2,相同温度下再次达到新平衡时SO3的物质的量为
2SO3(g),达到平衡时SO3为0.3 mol,此时若移走0.5 mol O2和0.5 mol SO2,相同温度下再次达到新平衡时SO3的物质的量为
A. 0.3 mol B. 0.15 mol
C. 小于0.15 mol D. 大于0.15 mol,小于0.3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种从铜电解工艺的阳极泥中提取Se和Te的流程如下:

下列叙述错误的是( )
A. 合理处理阳极泥有利于保护环境和资源再利用
B. 流出液是H2SO4溶液
C. 电解过程中阴极上析出单质Te
D. “焙砂”与碳酸钠充分混合后,可在瓷坩锅中焙烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组用如下图所示装置制备、收集Cl2,并进行性质验证实验(夹持装置略去)。下列说法正确的是( )

A. 用![]() 和浓盐酸制备
和浓盐酸制备![]() 时,只选
时,只选![]()
B. ![]() 用于
用于![]() 收集时,a为进气口
收集时,a为进气口
C. ![]() 中加入NaBr溶液和
中加入NaBr溶液和![]() ,通入
,通入![]() 反应后振荡、静置,下层溶液呈橙红色
反应后振荡、静置,下层溶液呈橙红色
D. ![]() 中通入
中通入![]() 使品红溶液褪色后,取出溶液加热可恢复红色
使品红溶液褪色后,取出溶液加热可恢复红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种自然界分布较广的元素,在很多化合物中都含有该元素,回答下列问题:


(1)装置A中反应的化学方程式为________________________________。
(2)使分液漏斗中液体顺利流下的操作是_______________________________________。
(3)选用上面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F的顺序连接装置即可证明,乙同学认为该方案不合理,其理由是___________________________________________。
②丙同学设计的合理实验方案为:A→C→____→____→D→F,其中装置C的作用是_______________,证明亚硫酸的酸性强于次氯酸的实验现象是___________________。
(4)K2S2O8具有强氧化性,可通过电解H2SO4和K2SO4的混合溶液制得,其阳极反应式为_______________,称取0.2500 g 产品于碘量瓶中,加100 mL水溶解,再加入8.000 g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以淀粉为指示剂,用 c mol/L的Na2S2O3标准液滴定至终点,消耗Na2S2O3标准液V mL,则样品中K2S2O8的纯度为_____%(用含c、V的代数式表示,已知:S2O82— +2I— = 2SO42—+I2 ;2S2O32— + I2 = 2S4O62—+2I— )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于四种基本反应类型但属于氧化还原反应的是
A.2FeCl3+Cu=2FeCl2+CuCl2
B.CuSO4+H2S=CuS↓+H2SO4
C.Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O
2CuO+CO2↑+H2O
D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是

A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图装置进行有关实验。请回答:
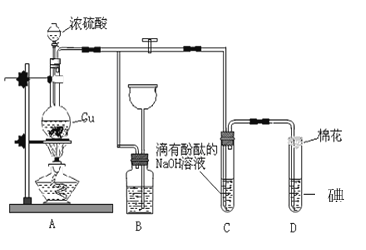
(1)装置A中发生的化学反应的化学方程式: _________________________________。
(2)装置B 的作用是__________________,B中广口瓶内应盛放的液体是_________(填序号)
①水 ②澄清石灰水
③Na2CO3溶液 ④饱和的NaHSO3 溶液
(3)装置C和D 中产生的现象相同,但原因却不同。C中反应的方程式:_______________________________________,而D 中则是由于SO2 具有_______性,D中反应的方程式:________________________。
(4)实验中,0.1molCu与含0.2mol硫酸的溶液反应后,铜和硫酸都有剩余。 可以证明有余酸的实验方案是___________
A.可再加入锌粒 B.可再加入氯化钡溶液
C.再加入银粉 D.再滴入碳酸氢钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为某化学反应速率一时间图。在t1时刻升高温度或增大压强,都符合图所示变化的反应是

A. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
B. 2SO2(g)+O2(g)![]() 2SO3(g)ΔH< 0
2SO3(g)ΔH< 0
C. H2(g)+I2(g)![]() 2HI(g)ΔH>0
2HI(g)ΔH>0
D. C(s)+H2O(g)![]() CO(g)+H2(g)ΔH>0
CO(g)+H2(g)ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com