
 的起还原剂作用,
的起还原剂作用,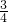 的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答.
的氨气中氮元素化合价不变,仅作为反应物参加反应.据此解答. 的起还原剂作用,被氧化,
的起还原剂作用,被氧化,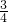 的氨气中氮元素化合价不变,仅作为反应物参加反应.
的氨气中氮元素化合价不变,仅作为反应物参加反应. :
: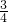 =1:3.
=1:3. 的起还原剂作用.
的起还原剂作用. 

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
A.NH3 16 mol B.NH3 8.0 mol
C.NH3 4.0 mol D.NH3 3.0 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NH3和Cl2可发生下列反应:8NH3+3Cl2====6NH4Cl+N2。若有2.0 mol N2生成,则发生氧化反应的物质及其物质的量分别是( )
A.NH3 16 mol B.NH3 8.0 mol
C.NH3 4.0 mol D.NH3 3.0 mol
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省内江市资中三中高一(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com