
| A£® | ŃÕÉ«±£³Ö²»±ä | |
| B£® | ĘųĢåĆܶȱ£³Ö²»±ä | |
| C£® | 2vÕż£ØHI£©=vÄę£ØI2£© | |
| D£® | ²šæŖ2 mol H-I¹²¼Ū¼ü£¬Ķ¬Ź±Éś³É1 mol H-H¹²¼Ū¼ü |
·ÖĪö øł¾Ż»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷½ā“š£¬µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷ĪļÖŹµÄÅØ¶Č”¢°Ł·Öŗ¬Įæ²»±ä£¬ŅŌ¼°ÓÉ“ĖŃÜÉśµÄŅ»Š©ĮæŅ²²»·¢Éś±ä»Æ£¬½āĢāŹ±ŅŖ×¢Ņā£¬Ń”ŌńÅŠ¶ĻµÄĪļĄķĮ棬Ėę×Å·“Ó¦µÄ½ųŠŠ·¢Éś±ä»Æ£¬µ±øĆĪļĄķĮæÓɱä»Æµ½¶ØÖµŹ±£¬ĖµĆ÷æÉÄę·“Ó¦µ½“ļĘ½ŗāדĢ¬£®
½ā“š ½ā£ŗA”¢»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁ±ä»Æ£¬ĖµĆ÷µāÕōĘųµÄÅØ¶Č²»±ä£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹAÕżČ·£»
B”¢¶ØČŻĆܱÕČŻĘ÷ÖŠ£¬»ģŗĻĘųĢåµÄÖŹĮæŗĶĢõ¼ž²»±ä£¬Ćܶȏ¼ÖÕŗć¶Ø²»±ä£¬²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹB“ķĪó£»
C”¢ĖŁĀŹÖ®±ČµČÓŚ»Æѧ·½³ĢŹ½¼ĘĖćÖ®±Č£¬ĪŖÕż·“Ó¦ĖŁĀŹÖ®±Č£¬2vÕż£ØHI£©=vÄę£ØI2£©²»·ūŗĻĖŁĀŹÖ®±ČµČÓŚ»Æѧ·½³ĢŹ½¼ĘĖ揿֮±Č£¬¹ŹC“ķĪó£»
D”¢µ„Ī»Ź±¼äÄŚ²šæŖ2molH-I¹²¼Ū¼ü£¬Ķ¬Ź±Éś³É1mol H-H£¬¶¼ŹĒÕżĻņ·“Ó¦£¬²»ÄÜČ·¶Ø ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬²»ÄÜČ·¶Ø“ļµ½ĮĖĘ½ŗāדĢ¬£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ£¬ĢāÄæÄŃ¶Č²»“ó£®ŅŖ×¢Ņā°ŃĪÕĘ½ŗāדĢ¬µÄĢŲÕ÷£¬×¢Ņāµ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | MgCl2 | B£® | K2S | C£® | LiCl | D£® | Na2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2 | B£® | C2H4 | C£® | ±½ | D£® | NaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K[Ag£ØCN£©2]”¢[Cu£ØNH3£©4]SO4 | B£® | [Ag£ØNH3£©2]Cl”¢K[Ag£ØCN£©2] | ||
| C£® | [Ag£ØNH3£©2]Cl”¢[Cu£ØNH3£©4]SO4 | D£® | [Ni£ØNH3£©4]Cl2”¢[Ag£ØNH3£©2]Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 3£¬3£¬4£¬6-Ėļ׻łŠĮĶé
3£¬3£¬4£¬6-Ėļ׻łŠĮĶé  3-¼×»ł-2-ŅŅ»ł-1-¶”Ļ©
3-¼×»ł-2-ŅŅ»ł-1-¶”Ļ© 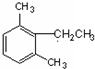 2£¬6-¶ž¼×»łŅŅ±½£®
2£¬6-¶ž¼×»łŅŅ±½£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ńõ»Æ»¹Ō·“Ó¦ŗĶĄė×Ó·“Ó¦ŹĒ֊ѧ»Æѧ֊ÖŲŅŖµÄ·“Ó¦ĄąŠĶ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
Ńõ»Æ»¹Ō·“Ó¦ŗĶĄė×Ó·“Ó¦ŹĒ֊ѧ»Æѧ֊ÖŲŅŖµÄ·“Ó¦ĄąŠĶ£®»Ų“šĻĀĮŠĪŹĢā£ŗ =2Cr£ØOH£©3”ż+3O2”ü+2H2O
=2Cr£ØOH£©3”ż+3O2”ü+2H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ijӊ»śĪļµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£¬øĆÓŠ»śĪļæÉÄÜ·¢ÉśµÄ·“Ó¦ŹĒ£Ø””””£©
ijӊ»śĪļµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£¬øĆÓŠ»śĪļæÉÄÜ·¢ÉśµÄ·“Ó¦ŹĒ£Ø””””£©| A£® | ¢Ł¢Ū¢Ü¢Ż¢Ž¢ß¢ą | B£® | ¢Ł¢Ś¢Ū¢Ü¢Ż¢Ž¢ą | C£® | ¢Ł¢Ś¢Ū¢Ž¢ą | D£® | ¢Ł¢Ū¢Ü¢Ż¢Ž¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀĮŗĻ½šŹĒÄæĒ°ÓĆĮæ×ī“ó”¢ÓĆĶ¾×ī¹ćµÄŗĻ½š | |
| B£® | ¶žŃõ»ÆĮņŹ¹Ę·ŗģČÜŅŗĶŹÉ«ŗĶŹ¹äåĖ®ĶŹÉ«µÄŌĄķĻąĶ¬ | |
| C£® | ČżÖÖ·ÖÉ¢ĻµÖŠ£¬½ŗĢåµÄĪČ¶ØŠŌ½éÓŚČÜŅŗŗĶ×ĒŅŗÖ®¼ä£¬ŹōÓŚ½éĪČĢåĻµ | |
| D£® | »īĘĆ½šŹōŌŚæÕĘųÖŠŅ×ÓėŃõĘų·“Ó¦£¬±ķĆęÉś³ÉŅ»²ćŃõ»ÆĪļ£¬¶ŌÄŚ²æ½šŹō¶¼ÄÜĘš±£»¤×÷ÓĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com